ΦΑΡΜΑΚΕΥΤΙΚΗ ΘΕΡΑΠΕΙΑ
ΤΗΣ ΓΥΝΑΙΚΕΙΑΣ ΑΚΡΑΤΕΙΑΣ
Iωάννης Βακαλόπουλος
Εισαγωγή
Παρά τις διάφορές, που υπάρχουν ανάμεσα στους ειδικούς για τη νευροφυσιολογία
και τη νευροφαρμακολογία του κατώτερου ουροποιητικού, όλοι συμφωνούν για το
ότι, στη φάση πλήρωσης της ουροδόχου κύστης, πρέπει να τηρούνται οι ακόλουθες
προϋποθέσεις:
- Πλήρωση της ουροδόχου κύστης με αυξανόμενο όγκο ούρων με χαμηλή πίεση και
με κατάλληλη αίσθηση ούρησης.
- Κλειστή έξοδος της κύστης στη φάση της πλήρωσης και παραμονή της σύγκλεισης
κατά την αύξηση της ενδοκοιλιακής πίεσης.
- Απουσία ακούσιων συστολών του εξωστήρα.
Τα φάρμακα, που χρησιμοποιούνται σήμερα στη θεραπεία της γυναικείας ακράτειας
δρουν επηρεάζοντας νευρωνικές οδούς, που ρυθμίζουν τη λειτουργία της κύστης
ή απευθείας πάνω στον εξωστήρα και στην πλειονότητα τους στερούνται εκλεκτικότητας
στη δράση τους, με συνέπεια να εμφανίζουν παρενέργειες, που περιορίζουν τη χρήση
τους, όταν χρησιμοποιούνται πάνω από κάποια ορισμένη δόση. Βελτίωση της ουροεκλεκτικότητας
των φαρμάκων μπορεί να επιτευχθεί με διάφορους τρόπους όπως:
Εκλεκτικότητα στους υποδοχείς, εκλεκτικότητα στο όργανο στόχο και εναλλακτικές
οδοί στην άφιξη του φαρμάκου στο όργανο (ενδοκυστική θεραπεία ή δερματικό επίθεμα),
στο μεταβολισμό (μείωση μεταβολίτη, που προκαλεί παρενέργειες) και/ή στην κατανομή
του φαρμάκου.
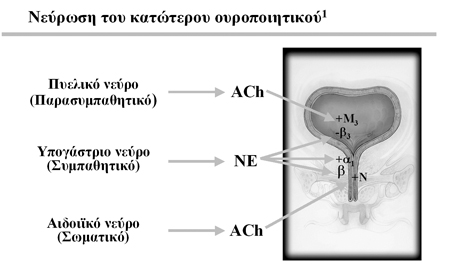
Εικόνα 1. Νεύρωση του κατώτερου
ουροποιητικού
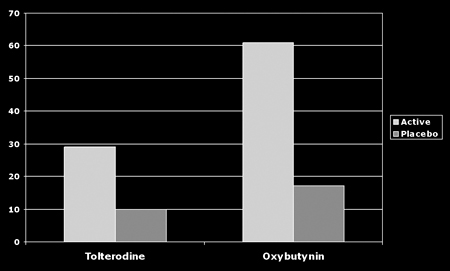
Εικόνα 2. Ποσοστά απόσυρσης
ασθενών από τη θεραπεία με τολτεροδίνη και οξυβουτινίνη λόγω ξηροστομίας σε
σχέση με το placebo.
Θεραπεία
που μειώνει τη συσταλτικότητα του εξωστήρα
Α) Αμιγή αντιχολινεργικά φάρμακα
Τα φάρμακα αυτά δρουν μπλοκάροντας τους μουσκαρινικούς υποδοχείς των μεταγαγγλιακών
νευρικών ινών του παρασυμπαθητικού στον εξωστήρα μυ και αναστέλλουν έτσι τις
φυσιολογικές και ανεπιθύμητες συστολές του εξωστήρα[1]. Η φαρμακολογική δράση
αυτών των ουσιών έγκειται στα ακόλουθα αποτελέσματα:
- Αυξάνουν τον ουδό του όγκου και της πίεσης των ούρων ως την εμφάνιση μιας
ανεπιθύμητης συστολής του εξωστήρα και μειώνουν το πλάτος της.[2]
- Αυξάνουν την κυστική χωρητικότητα
- Μειώνουν την αίσθηση της έπειξης μειώνοντας τον τόνο της κύστης κατά την πλήρωση
- Δεν μεταβάλλουν την ικανότητα καταστολής μιας ανεπιθύμητης συστολής καθώς
και το "χρόνο προειδοποίησης" της, δηλαδή το χρόνο, που μεσολαβεί
από την έναρξη αντίληψης της συστολής ως το χρόνο εμφάνισης της.
Φυσιολογικά υπάρχουν 5 υπότυποι μουσκαρινικών υποδοχέων, που χαρακτηρίζονται
ως Μ1-Μ5. Ο ανθρώπινος εξωστήρας περιλαμβάνει κατά 80% Μ2 υποδοχείς και κατά
20% Μ3.3 (Εικόνα 1) Ωστόσο, οι Μ3 υποδοχείς είναι οι κυρίως υπεύθυνοι για τη
συστολή του εξωστήρα. Αν και τα φάρμακα, που είναι εκλεκτικά για τους υποδοχείς
αυτούς, έχουν λιγότερες παρενέργειες από τα μη εκλεκτικά φάρμακα, οι Μ3 υποδοχείς
του εξωστήρα είναι ίδιοι με τους Μ3 υποδοχείς, που υπάρχουν και σε άλλα όργανα.[4]
Για το λόγο αυτό γίνεται έρευνα για την ανεύρεση φαρμάκων, που θα εκμεταλλεύονται
μια πιθανή ετερογένεια των Μ3 υποδοχέων, που ρυθμίζουν τη κυστική συσταλτικότητα,
ώστε οι πιθανές παρενέργειες να μειώνονται ακόμη περισσότερο. Οι συνήθεις παρενέργειες
των αντιχολινεργικών φαρμάκων είναι ξηροστομία, διπλωπία, ταχυκαρδία, δυσκοιλιότητα,
ανιδρωσία, δυσχέρεια ούρησης και παρενέργειες από το ΚΝΣ. Γενικά αντενδείκνυνται
απόλυτα σε ασθενείς με γλαύκωμα κλειστής γωνίας και πρέπει να χορηγούνται με
προσοχή σε ασθενείς με δυσχέρεια ούρησης. (Εικόνα 2) Τα συνηθέστερα χρησιμοποιούμενα
φάρμακα αυτής της κατηγορίας είναι:
1) Τολτεροδίνη
Μη εκλεκτική δράση στους μουσκαρινικούς υποδοχείς, αλλά καλά ανεκτή όσον αφορά
τη ξηροστομία (2%-10%),δυσκοιλιότητα(7%),και παρενέργειες από το ΚΝΣ.[5] Τα
επεισόδια ακράτειας από έπειξη μειώνονται κατά 40%-60% και της συχνουρίας 20%.[6]
2) Trospium Chloride
Παρόμοιο με την οξυβουτινίνη με λιγότερες παρενέργειες
3) Νταριφενακίνη, Σολιφενακίνη
Υψηλή εκλεκτικότητα για τους Μ3 υποδοχείς. Φαίνεται να έχει παρόμοια ουροδυναμική
δράση δράση με την οξυβουτινίνη, αλλά σημαντικά μικρότερη μείωση της ροής σιέλου.
Όπως προκύπτει από τις μελέτες της φάσης 3 το ποσοστό απόσυρσης λόγω ανεπιθύμητων
ενεργειών από τη σολιφενακίνη ανέρχεται στο 3.5%.7 (Εικόνες 3,4)
Α.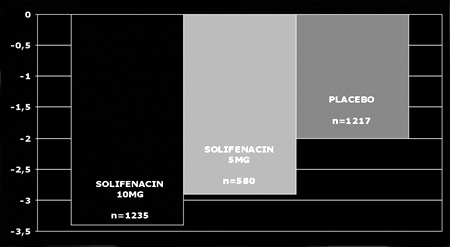
Β.
Εικόνα 3. Ποσοστά μείωσης της έπειξης Α)και της ακράτειας Β) με σολιφενακίνη
σε σχέση με το placebo
Β) Αντιχολινεργικά μεικτής
δράσης
Τα φάρμακα αυτά έχουν εκτός από την μη εκλεκτική αντιμουσκαρινική τους δράση
και μια άμεση μυοτρόπο δράση προκαλώντας χάλαση του εξωστήρα, αλλά και μια τοπική
αναισθητική δράση. Ωστόσο, στην από του στόματος χορήγηση δρουν μόνο μέσω μουσκαρινικού
μπλοκαρίσματος, ενώ οι άλλες δράσεις εμφανίζονται σε πολύ υψηλότερες δόσεις,
εκτός εάν χορηγηθούν με ενδοκυστική έγχυση. Ο σημαντικότερος εκπρόσωπος τους
είναι η οξυβουτινίνη. Η οξυβουτινίνη μειώνει την ακράτεια από έπειξη κατά 52%,
τη συχνουρία κατά 33%, ενώ επιφέρει συνολική υποκειμενική βελτίωση στην υπερδραστήρια
κύστη κατά 74%. Το ποσοστό παρενεργειών φθάνει κατά μέσο όρο το 70%(17%-93%)8
και η απόσυρση το 3%-45%.[9]
Εκτός από τη συνήθη μορφή σε δισκία των 5mg, που χορηγούνται τρεις φορές ημερησίως,
άλλες μορφές του φαρμάκου περιλαμβάνουν δισκία ημερήσιας χορήγησης, δερματικό
patch,[10] ενδοκυστική χρήση και διορθική χρήση. Οι μορφές αυτές έχουν παρόμοια
αποτελεσματικότητα με ην κλασσική χορήγηση, αλλά με λιγότερες παρενέργειες.
Γ) Άλλα φάρμακα που μειώνουν
τη συσταλτικότητα του εξωστήρα με διάφορες δράσεις
- Ανταγωνιστές ασβεστίου
- Φάρμακα, που προκαλούν άνοιγμα των καναλιών καλίου
- Ανταγωνιστές των προσταγλανδινών
- β- αδρενεργικοί αγωνιστές
- α- αδρενεργικοί ανταγωνιστές
- Τρικυκλικά αντικαταθλιπτικά
Από τα παραπάνω μόνο τα τρικυκλικά αντικαταθλιπτικά ιμιπραμίνη και αμιτρυπτιλίνη
έχουν τύχει κάποιας ευρύτερης εφαρμογής στη θεραπεία της υπερδραστήριας κύστης.
Τα φάρμακα αυτά αυξάνουν την αντίσταση εξόδου των ούρων και μειώνουν τη συσταλτικότητα
του εξωστήρα προκαλώντας την αύξηση της αποθηκευτικής ικανότητας της κύστης.[11]
Η ιμιπραμίνη έχει άμεση μυοχαλαρωτική δράση στον εξωστήρα πιθανώς αναστέλλοντας
την επαναπρόσληψη της σεροτονίνης στο ΚΝΣ. Περιορίζει την ακράτεια από έπειξη
σε ποσοστό 20%-77%, ενώ παρενέργειες αναφέρονται σε ποσοστό 0%-70%.[9]
Θεραπεία, που μειώνει
την αισθητικότητα της κύστης
Η μείωση της αισθητικής οδού μεταφοράς ερεθισμάτων έπειξης προς ούρηση
θα ήταν ιδανική σε περιπτώσεις, όπου η ελαστικότητα του εξωστήρα είναι φυσιολογική,
δεν υπάρχουν ουροδυναμικές ενδείξεις υπερδραστηριότητας και και το αισθητικό
σκέλος προεξάρχει σε μια διαταραχή του αντανακλαστικού ούρησης. Τα φάρμακα,
που μειώνουν την αισθητικότητα της ουροδόχου κύστης, λέγονται βανιλλοειδή, λόγω
της μορφής του μορίου τους και είναι η καψαϊσίνη και η ρεσινφερατοξίνη. Η καψαϊσίνη
προέρχεται από τις κόκκινες πιπεριές και δρα στον υποδοχέα Ι των βανιλλοειδών
μπλοκάροντας την αγωγή των C νευρικών ινών, διακόπτοντας έτσι τη μεταφορά του
επώδυνου ερεθίσματος και μειώνοντας τη νευρογενή φλεγμονή.[12]
Αν και ιδιαίτερα ερεθιστική αρχικά, φαίνεται αποτελεσματική σε σχέση με το placebo.[13]
Η ρεσινφερατοξίνη προέρχεται από τον κάκτο Euphorbia Resinfera και είναι βανιλλοειδές
ισχυρότερο από την καψαϊσίνη και με μικρή ερεθιστική δράση. Κανένα από τα δύο
φάρμακα δεν είναι εγκεκριμένο για χρήση στις ΗΠΑ προς το παρόν, αν και η ενδοκυστική
χορήγηση τους μπορεί να συνεισφέρει στη θεραπεία κάποιων μορφών αισθητικής έπειξης
και οι μελέτες για την ρεσινφερατοξίνη συνεχίζονται.

Εικόνα 4. Παρενέργειες της
σολιφενακίνης σε σχέση με το placebo
Α.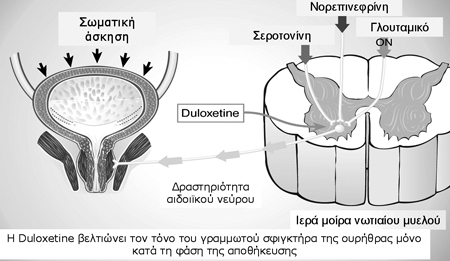
Β.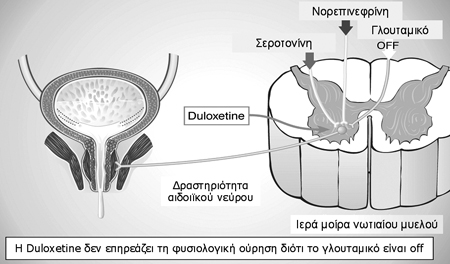
Εικόνα 5. Α) Στη φάση της πλήρωσης της ουροδόχου κύστης η ντουλοξετίνη προκαλεί
αύξηση των επιπέδων σεροτονίνης και νορεπινεφρίνης στον πυρήνα του αιδοιικού
νεύρου αναστέλλοντας την επαναπρόσληψη τους. Τα αυξημένα αυτά επίπεδα παρουσία
γλουταμικού οξέος προκαλούν αύξηση της δραστηριότητας του αιδοιϊκού νεύρου και
έτσι αύξηση της σύσπασης του γραμμωτού σφιγκτήρα της ουρήθρας και παρεμπόδιση
της ακούσιας διαφυγής κατά την αύξηση της ενδοκοιλιακής πίεσης.
Β) Στη φάση της κένωσης διακόπτεται η έκκριση γλουταμικού
με συνέπεια την αναστολή της δράσης της σεροτονίνης και νορεπινεφρίνης και έτσι
αναστολή της δράσης του αιδοιϊκού νεύρου, χάλαση του σφιγκτήρα και ομαλή ούρηση,
ένα πλεονέκτημα, που στερούνται οι α αγωνιστές, οι οποίοι δρουν και στις δύο
φάσεις της λειτουργίας της κύστης, παρεμποδίζοντας έτσι τη φυσιολογική ούρηση.
Α.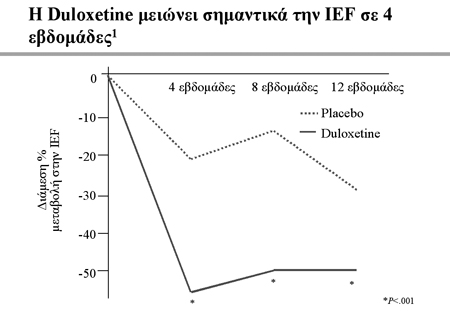
Β.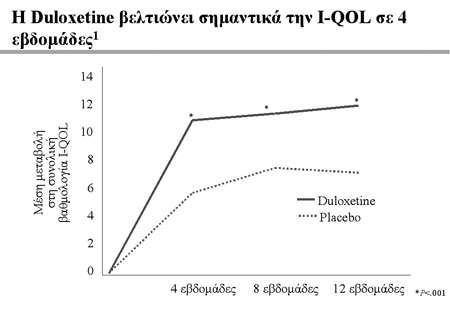
Εικόνα 6. Α) Μείωση των επεισοδίων
ακράτειας με τη ντουλοξετίνη σε σχέση με το placebo Β) Βελτίωση της ποιότητας
ζωής με τη ντουλοξετίνη σε σχέση με το placebo
Θεραπεία για
την αύξηση των αντιστάσεων εξόδου των ούρων με εφαρμογή στην ακράτεια από προσπάθεια
Πριν την πρόσφατη χρήση της υδροχλωρικής ντουλοξετίνης για τη θεραπεία της ακράτειας
από προσπάθεια χρησιμοποιούνταν διάφορα φάρμακα, κυρίως συμπαθητικομιμητικά,
από τα οποία μόνο ελάχιστα είχαν λάβει ένδειξη σε κάποιες χώρες και όχι στην
Ελλάδα. Ορισμένα από αυτά χρησιμοποιούνται ακόμη, αν και η χρήση τους μετά την
εμφάνιση της ντουλοξετίνης έχει περιορισθεί σημαντικά και πιθανώς θα σταματήσει,
αφού υπάρχει φάρμακο με συγκεκριμένη ένδειξη.
Ο αυχένας της κύστης και η εγγύς ουρήθρα είναι πλούσιοι σε α1 υποδοχείς του
συμπαθητικού, που με την ενεργοποίηση τους προκαλούν σύσπαση των λείων μυϊκών
ινών. Διάφορα φάρμακα από το στόμα έχουν α αδρενεργική δράση και η λήψη τους
προκαλεί αύξηση της αντίστασης εξόδου των ούρων και ουροδυναμικά, αύξηση της
πίεσης σύγκλεισης της ουρήθρας. Παραδείγματα τέτοιων φαρμάκων είναι η εφεδρίνη,
η φαινυλεφρίνη, η μιδοδρίνη και η φαινυλοπροπανολαμίνη. Η συνδυασμένη μετανάλυση
οκτώ μελετών για την τελευταία αναδεικνύει θεραπεία της ακράτειας από προσπάθεια
σε ποσοστά 0%-14%, μείωση των επεισοδίων ακράτειας 19%-60%, εμφάνιση παρενεργειών
5%-33% και διακοπή της θεραπείας 0%-4.3%.9 Τα φάρμακα αυτά μπορεί να προκαλέσουν
αύξηση της αρτηριακής πίεσης και της καρδιακής συχνότητας και ενίοτε τρόμο,
διαταραχές του ύπνου, κεφαλαλγία, αίσθημα παλμών, αγγειακό εγκεφαλικό επεισόδιο
και θάνατο. Ερευνητική προσπάθεια καταβάλλεται για την ανεύρεση εκλεκτικών για
το ουροθήλιο αδρενεργικών αγωνιστών, ώστε να αποφεύγονται οι σοβαρές παρενέργειες
από το καρδιαγγειακό.
Η δράση των τρικυκλικών αντικαταθλιπτικών με κύριο εκπρόσωπο την ιμιπραμίνη
και στην Ελλάδα την αμιτρυπτιλίνη έχει ήδη προαναφερθεί στη αντιμετώπιση της
υπερδραστήριας κύστης. Σε μια ανοιχτή μελέτη ο Lin και συνεργάτες ανέφεραν,
ότι 25mg ιμιπραμίνης 3 φορές ημερησίως για 3 μήνες οδήγησαν σε θεραπεία το 35%
των γυναικών, που έπασχαν από ακράτεια από προσπάθεια. Σε ένα 25% επιπρόσθετα
υπήρχε πάνω από 50% βελτίωση. Η βελτίωση φάνηκε να συσχετίζεται με την αύξηση
της πίεσης σύγκλεισης της ουρήθρας.[14]
Στις μετεμμηνοπαυσιακές γυναίκες παρατηρείται μια αύξηση των συμπτωμάτων του
κατώτερου ουροποιητικού, συμπεριλαμβανομένης της ακράτειας και των ουρολοιμώξεων.
Το ερώτημα είναι εάν τα ευρήματα αυτά σχετίζονται με την έλλειψη οιστρογόνων.
Οι θεωρητικές επιδράσεις, που μπορεί να έχει μια θεραπεία με οιστρογόνα αμιγώς
ή επικουρικά, στηρίζονται στις εξής δράσεις των οιστρογόνων:
Ασκούν τροφική δράση στο επιθήλιο της ουρήθρας και στο κολλαγόνο του ουρηθρικού
και περιουρηθρικού ιστού και αυξάνουν την υποεπιθηλιακή αγγειοβρίθεια, αυξάνουν
τη συγκέντρωση των α αδρενεργικών υποδοχέων στις λείες μυϊκές ίνες της ουρήθρας
και την ευαισθησία τους στην α αδρενεργική δράση. Η τελική γνώμη των Hextal[15]
και Anderson[16] μετά από μια πρόσφατη βιβλιογραφική ανασκόπηση στην χρήση των
οιστρογόνων για τη θεραπεία των συμπτωμάτων του κατώτερου ουροποιητικού είναι,
ότι η χρήση τους μάλλον δεν ωφελεί τη θεραπεία της ακράτειας από προσπάθεια
και από έπειξη, πιθανώς να ωφελεί στην καταπολέμηση της συχνουρίας και έπειξης
και ωφελεί στη θεραπεία των υποτροπιαζουσών ουρολοιμώξεων και ιδίως τα κολπικά
σκευάσματα.
Υδροχλωρική
Ντουλοξετίνη
Η υδροχλωρική ντουλοξετίνη είναι ένα νέο φάρμακο με ένδειξη τη θεραπεία της
αμιγούς ακράτειας από προσπάθεια. Το φάρμακο είναι ένας ισορροπημένος αναστολέας
της επαναπρόσληψης της σεροτονίνης και νορεπινεφρίνης in vivo και in vitro στο
Κεντρικό Νευρικό Σύστημα, ενώ δεν έχει καμία συγγένεια για τους χολινεργικούς
υποδοχείς.[17] Το φάρμακο δρα και στον πυρήνα του Onuf, πυρήνα του αιδοιϊκού
νεύρου στην ιερά μοίρα του νωτιαίου μυελού (Ι2-Ι4). Το αιδοιϊκό νεύρο ρυθμίζει
τη λειτουργία του γραμμωτού σφιγκτήρα της ουρήθρας. Το φάρμακο αναστέλλοντας
την επαναπρόσληψη της σεροτονίνης και της νορεπινεφρίνης, αυξάνει την ενεργοποίηση
των α1 αδρενεργικών υποδοχέων, καθώς και των 5-ΗΤ2 υποδοχέων, αυξάνοντας έτσι
τη δραστηριότητα του αιδοιϊκού νεύρου και οδηγώντας έτσι στην ισχυρότερη σύγκλειση
του σφιγκτήρα στη φάση πλήρωσης της κύστης, εμποδίζοντας με αυτό τον τρόπο την
ανεπιθύμητα διαφυγή ούρων.[18] Η δράση αυτή πραγματοποιείται παρουσία γλουταμικού
οξέος, που απελευθερώνεται ως νευροδιαβιβαστής από ανώτερα κέντρα. Στη φάση
της κένωσης η έκκριση γλουταμικού οξέος αναστέλλεται και έτσι η ντουλοξετίνη
παύει να δρα, επιτρέποντας με αυτό τον τρόπο την ομαλή ροή των ούρων.[19] (Εικόνα
5)
Σε μια πρόσφατη μελέτη του Dmochowski και συνεργατών μελετήθηκαν 683 γυναίκες
με αμιγή ακράτεια από προσπάθεια. Τα αποτελέσματα έδειξαν στατιστικά σημαντική
μείωση στην εβδομαδιαία συχνότητα επεισοδίων ακράτειας σε σχέση με το placebo
(50% σε σχέση με 27%), αύξηση στα μεσοδιαστήματα ούρησης και ταυτόχρονη βελτίωση
στην ποιότητα ζωής.(Εικόνα 6) Οι μισές γυναίκες της μελέτης παρουσίασαν μείωση
των επεισοδίων ακράτειας από 51%-100%. Το ποσοστό απόσυρσης λόγω ανεπιθύμητων
ενεργειών ήταν 24% με τη ναυτία να είναι η κύρια αιτία. Ωστόσο, η ναυτία είναι
παροδική και εξαφανίζεται σε διάστημα από μια εβδομάδα ως ένα μήνα.[20] Η σταδιακή
επίσης αύξηση της δόσης του φαρμάκου από τα 20mg στα 40 mg μετά από ένα μήνα
θεραπείας μειώνει σημαντικά το ποσοστό απόσυρσης λόγω ναυτίας. Δυσκοιλιότητα
και ξηροστομία μπορεί να παρατηρηθούν, χωρίς να είναι σημαντικές αιτίες απόσυρσης.
Βιβλιογραφία
1. Andersson K-E. Advances
in the pharmacological control of the bladder. Exp Phys 1999, 84:195-213.
2. Jensen Jr D. Pharmacological studies of the uninhibited neurogenic bladder.
II. The influence of cholinergic excitatory and inhibitory drugs on the cystometrogram
of neurological patients with normal and uninhibited neurogenic bladder. Acta
Neurol Scand 1981, 64:175-195.
3. Chapple C. Muscarinic receptor antagonists in the treatment of overactive
bladder. Urology 2000, 55: 33-46.
4. Caulfield MP, Birdshall NJ. International Union of Pharmacology XVII. Classification
of muscarinic achetylocholine receptors. Pharmacol Rev. 1998, 50: 279-290.
5. Chancelllor M, Freedman S. Tolterodine an effective and well tolerated treatment
for urge incontinence and other overactive bladder symptoms. Clinical Drug Investigation
2000, 19: 83-91.
6. Appel R. Clinical efficacy and safety of tolterodine in the treatment of
overactive bladder. A pooled analysis. Urology 1997, 50: 90-99.
7. Data on file: Integrated Analysis of Safety of Solifenacin (January 2003)
plus individual study reports CL-015 and CL-018
8. Thuroff J, Abrams P, Chartier-Kasher E, et al. Medical treatment and medical
side effects in urinary incontinence in the elderly. World J Urology 1998, 16:
548-61
9. Agency for Health Care Policy and Research. Urinary incontinence Guide Line
Panel. Urinary Incontinence in Adults: Clinical Practice Guidelines (edAHCPR
publication#92-0038). Rockville, MD, Public Health Service, US. Department of
Health and Human Services, 1992.
10. Davila GW, Daugherty CA, Sanders SW, et al. A sort term, multicenter, randomized,
double blind, dose titration study of the efficacy and anticholinergic side
effects of transdermal compared to immediate release oral oxyboutinin treatment
of patients with urge urinary incontinence, J Urol 2001, 166: 140-145.
11. Wein AJ. Pharmacology of Incontinence. Urol Clin N Am 1995, 22: 557-577
12. Dray A. Mechanism of action of capsaicin like molecules on sensory Neurons.
Life Sci 1992, 51:1759-1765.
13. DeRidder D, Baert L. vanilloids and the overactive bladder. BJU International
2000, 86:172-180.
14. Lin H-H, Sheu BC, Lo M-C. Comparison of treatment outcomes of imipramine
for female genuine stress incontinence. Brit J Obstet Gynecol 1999, 106: 1089-1092.
15. Hextall A. Oestregens and lower urinary tract functions. Maturitas 2000,
36: 83-87.
16. Andersson K-E, Appel R, Awad S, et al. Pharmacological treatment of urinary
incontinence. In Abrams P, Khoury S, Cardoso L, et al, editors. Incontinence.
Plymouth, UK: Health Publications, 2002.
17. Lantz RJ et al. Metabolism, excretion and pharmacocinetics of Duloxetine
in healthy human subjects. Drum Metabolism and Disposition 2003, 31: 1142-1150.
18. Kreder K et al. Eur Urol 2002, 41(6) 588
19. Thor KB, et al. J Pharmacol Exp Ther 1995, 274(2): 1014-1024
20. Dmochowski R, Miklos J, Norton P, Zinner N, Yalcin I, Bump R. Duloxetine
versus placebo for the treatment of North American women with stress urinary
incontinense. J Urol 2003, 170:1259 1263