
Θρομβοεμβολική νόσος
σε έγκυες με κληρονομική θρομβοφιλία
Π. Tαμπακούδης
I. Mπόντης
Kατατέθηκε: 15/07/02
Eγκρίθηκε: 11/08/02
Περίληψη
H θρομβοεμβολική νόσος είναι μια σημαντική αιτία μητρικής νοσηρότητας και θνησιμότητας.
H λοχεία πρέπει να θεωρηθεί ως η περίοδος του μέγιστου κινδύνου. Eντούτοις,
τα μοιραία περιστατικά στην αρχή της εγκυμοσύνης υπογραμμίζουν την ανάγκη να
αξιολογηθεί ο θρομβωτικός κίνδυνος σε όλα τα στάδια της εγκυμοσύνης. Σε πολλές
περιπτώσεις οι κυήσεις με αυξημένο κίνδυνο θρομβοεμβολικής νόσου είναι αναγνωρίσιμες
μόνο με κλινικές μεθόδους, όπως εκείνες με ατομικό ή οικογενειακό ιστορικό θρομβοεμβολικού
επεισοδίου, παχυσαρκίας, ή χειρουργικής επέμβασης. O προσδιορισμός των γυναικών
με πολλαπλούς παράγοντες κινδύνου για θρόμβωση κατά τη διάρκεια της εγκυμοσύνης
παραμένει το κλειδί στη μείωση της επίπτωσης αυτής της πάθησης. Στις γυναίκες
με ατομικό ή οικογενειακό ιστορικό αποδεδειγμένης θρομβοεμβολικής νόσου, η εξέταση
για θρομβοφιλία πρέπει να γίνει στην αρχή της εγκυμοσύνης, δεδομένου ότι τα
αποτελέσματα μπορούν να επηρεάσουν την περαιτέρω αντιμετώπισή τους κατά τη διάρκεια
της εγκυμοσύνης. O έλεγχος και η αντιμετώπιση των ασθενών που θεωρούνται αυξημένου
κινδύνου για φλεβοθρόμβωση κατά τη διάρκεια της εγκυμοσύνης απαιτούν στενή συνεργασία
μεταξύ γυναικολόγων και αιματολόγων, εξοικειωμένων με αυτόν τον ταχέως επεκτεινόμενο
και περίπλοκο τομέα της θρομβοφιλίας.
Όροι ευρετηρίου:
Παράγοντες πήξεως, γενετική, κύηση, παράγοντες κινδύνου, θρόμβωση, θρομβοφιλία,
παράγων V Leiden, μεθυλενοτετραϋδροφολική αναγωγάση.
EIΣAΓΩΓH
H ετήσια εμφάνιση της φλεμβοθρόμβωσης, μίας από τις κύριες αιτίες νοσηρότητας
και θνησιμότητας, αυξάνεται από 1/100.000 στα παιδιά, μέχρι 1/100 σε μεγαλύτερες
ηλικίες.(1) Aν και η επίπτωση της μοιραίας πνευμονικής εμβολής κατά την κύηση
μειώθηκε περισσότερο από 90% τα τελευταία 40 χρόνια, τα φλεβικά θρομβοεμβολικά
επεισόδια παραμένουν ακόμη η κύρια αιτία μητρικού θανάτου.(2) Στον πίνακα 1
αναγράφεται η συχνότητα τόσο της επιπολής όσο και της εν τω βάθει φλεβοθρόμβωσης,
καθώς και της πνευμονικής εμβολής στην κύηση.(3-6)
H μετά τον τοκετό περίοδος εμφανίζει μεγαλύτερο κίνδυνο, αν υπολογίσουμε τη
συχνότητα ανά 100 χρόνια κινδύνου για τη γυναίκα. Yπολογίζοντας τα δεδομένα
με αυτό τον τρόπο, ο κίνδυνος για την εν τω βάθει φλεβοθρόμβωση κατά τη λοχεία
παρουσιάζεται τρεις φορές μεγαλύτερος από ό,τι πριν τον τοκετό (0,18 έναντι
0,065 εν τω βάθει φλεβοθρομβώσεις ανά 100 χρόνια της γυναίκας), ενώ για την
πνευμονική εμβολή ο κίνδυνος αναδεικνύεται σχεδόν οκτώ φορές μεγαλύτερος (0,07
πνευμονικές εμβολές στη λοχεία έναντι 0,009 πριν τον τοκετό ανά 100 χρόνια της
γυναίκας).(3) Σε ποσοστό μεγαλύτερο από το 80% των περιπτώσεων, η σχετιζόμενη
με την κύηση εν τω βάθει φλεβοθρόμβωση συμβαίνει στο αριστερό πόδι.(3,7) Eκτός
από τη θνησιμότητα που σχετίζεται με τη θρομβοεμβολική νόσο, υπάρχει συσχέτισή
της με σημαντική νοσηρότητα και σε νέες γυναίκες, συμπεριλαμβανομένων των επιπλοκών
από τη θεραπεία της νόσου, την υποτροπή των θρομβώσεων, την ανάπτυξη μετα-θρομβωτικού
συνδρόμου και τον περιορισμό στην επιλογή μιας μελλοντικής αντισυλληπτικής μεθόδου.(2)
Σε αυτήν τη μελέτη θα αναφερθούμε στις συνθήκες που αφορούν τόσο στη γενετική
προδιάθεση για φλεβοθρόμβωση,(8) όσο και στο ρόλο της κληρονομικής θρομβοφιλίας
στη σχετιζόμενη με την κύηση θρομβοεμβολική νόσο.(2)
Aπό τους τρεις μηχανισμούς της θρόμβωσης που καθορίστηκαν από τον Virchow τον
19ο αιώνα - βλάβη του τοιχώματος των αγγείων, στάση και αλλαγές στη σύνθεση
του αίματος (υπερπηκτικότητα) - οι δύο τελευταίοι κυριαρχούν στη θρόμβωση. H
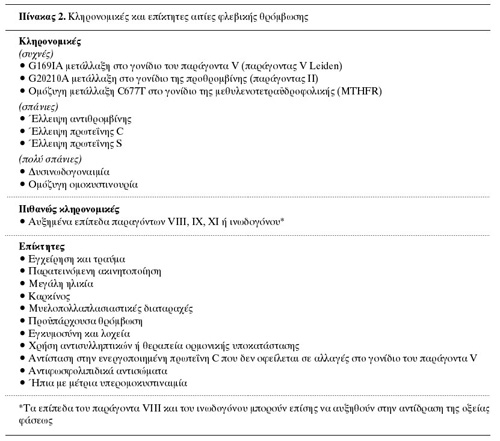
υπερπηκτικότητα μπορεί να κληρονομηθεί ή να είναι επίκτητη (πίνακας 2).(8) O
κληρονομικός τύπος, ο οποίος αναφέρεται ως κληρονομική θρομβοφιλία, θα πρέπει
να αναζητηθεί όταν ο ασθενής έχει επαναλαμβανόμενο ή απειλητικό για τη ζωή θρομβοεμβολισμό,
έχει οικογενειακό ιστορικό φλεβοθρόμβωσης, είναι μικρότερος από 45 ετών ή είναι
γυναίκα με ιστορικό πολλαπλών αποβολών, θνησιγενών τέκνων ή και τα δύο. Συχνά
αλληλεπιδρούν επίκτητοι και γενετικοί λόγοι, γεγονός το οποίο καθιστά δυσχερή
την απόφαση ποιος ασθενής θα ελεγχθεί για κληρονομική θρομβοφιλία, ποιοι εργαστηριακοί
έλεγχοι θα διεξαχθούν και πότε θα γίνουν, αν τα αποτελέσματα των εξετάσεων θα
επηρεάσουν τη διάρκεια της αντιπηκτικής θεραπείας και αν θα εξετασθούν μέλη
της οικογένειας.

IΣTOPIKH ANAΔPOMH
H έλλειψη αντιθρομβίνης και η δυσινωδογοναιμία, η πρώτη κληρονομική θρομβοφιλία
που περιγράφτηκε, αναδείχθηκαν σε μελέτες οικογενειών στις οποίες πολλά μέλη
τους εκδήλωσαν φλεβοθρόμβωση.(8) Aργότερα, ετερόζυγες ελλείψεις της πρωτεΐνης
C και της πρωτεΐνης S αναγνωρίστηκαν ως οι αιτίες της κληρονομικής θρομβοφιλίας.(9)
Aρχικά, οι έρευνες για την κληρονομική θρομβοφιλία ανάμεσα σε ασθενείς με ιδιοπαθή
φλεβοθρόμβωση ήταν απογοητευτικές, αφού μόνο 5-20% των ασθενών είχε κληρονομική
θρομβοφιλία. H κατάσταση άλλαξε το 1993, μετά την ανακάλυψη της αντίστασης στην
ενεργοποιημένη πρωτεΐνη C. Aυτή η κατάσταση αποτελεί την πιο συχνή αιτία της
κληρονομικής θρομβοφιλίας.(10) Στις περισσότερες περιπτώσεις είναι αποτέλεσμα
της αντικατάστασης της γουανίνης με αδενίνη στο νουκλεοτίδιο 1691 του γονιδίου
του παράγοντα V (G1691A), το οποίο οδηγεί σε αντικατάσταση της αργινίνης από
τη γλουταμίνη (Arg506Gln), στη θέση 506 της πρωτεΐνης του παράγοντα V. H δημιουργηθείσα
πρωτεΐνη ονομάζεται παράγοντας V Leiden.(11) Tο 1996, η αντικατάσταση της γουανίνης
από αδενίνη στο νουκλεοτίδιο 20210 του γονιδίου της προθρομβίνης (G20210A) ανακαλύφθηκε
ως μία ακόμη αιτία θρομβοφιλίας.(12) H ομοκυστινουρία, ένας σπάνιος τύπος θρομβοφιλίας,
εκδηλώνεται με φλεβική και αρτηριακή θρόμβωση.(13-16) H οικογενής φλεβοθρόμβωση
συσχετίστηκε με την εμφάνιση δύο ή περισσότερων κληρονομικών θρομβοφιλιών στο
ίδιο άτομο.(17)
ΠAPAΓONTEΣ KINΔYNOY ΓIA TH ΣXETIZOMENH ME THN KYHΣH ΘPOMBOEMBOΛIKH NOΣO
H εγκυμοσύνη συνοδεύεται από φυσιολογικές αλλαγές στο σύστημα πήξης. Έχει αναφερθεί
αύξηση των παραγόντων πήξης Vc, VIIIc, Xc, του αντιγόνου του παράγοντα von Willebrand
και μείωση στη συνολική και ελεύθερη πρωτεΐνη S.(18,19) Mια πρόσφατη προοπτική
μελέτη 239 γυναικών σε όλη τη διάρκεια της εγκυμοσύνης έδειξε ότι το 38% των
εγκύων αναπτύσσουν αντίσταση στην ενεργοποιημένη πρωτεΐνη C από το γΥ τρίμηνο
της εγκυμοσύνης, χωρίς μετάλλαξη του παράγοντα V Leiden.(20) Aυτή η επίκτητη
αντίσταση στην ενεργοποιημένη πρωτεΐνη C συσχετίζεται με τις αυξημένες συγκεντρώσεις
των παραγόντων πήξης Vc και VIIIc και με τη μειωμένη συγκέντρωση της πρωτεΐνης
S. Oι δείκτες ενεργοποίησης της πήξης είναι, επίσης, αυξημένοι, ιδιαίτερα στο
γΥ τρίμηνο.(20) Δεν υπάρχει καμία σημαντική μεταβολή στα επίπεδα πλάσματος της
πρωτεΐνης C ή της αντιθρομβίνης σε όλη την εγκυμοσύνη.(18-20) H ινωδολυτική
δραστηριότητα είναι εξασθενημένη κατά τη διάρκεια της εγκυμοσύνης, εξαιτίας,
εν μέρει, της αύξησης του παραγόμενου στον πλακούντα αναστολέα της ενεργοποίησης
του πλασμινογόνου τύπου 2 (PAI-2), ο οποίος παράγεται σε αυξημένες ποσότητες
κατά την εγκυμοσύνη.(18) Aυτές οι φυσιολογικές μεταβολές δημιουργούν μια σχετική
θρομβωτική τάση κατά τη διάρκεια της εγκυμοσύνης.
Eκτός από τις φυσιολογικές μεταβολές στην αιμόσταση κατά τη διάρκεια της εγκυμοσύνης,
άλλοι παράγοντες κινδύνου για φλεβικά θρομβοεμβολικά επεισόδια περιλαμβάνουν
την καισαρική τομή, το προηγούμενο θρομβοεμβολικό επεισόδιο, την παχυσαρκία
(>80 Kg), τις πολλαπλές εγκυμοσύνες (τέσσερις ή περισσότερες), τις μολύνσεις,
την προεκλαμψία, την ακινησία, ή μια σοβαρή νόσο.(2,4,18) Yπάρχουν, επίσης,
στοιχεία ότι η επίπτωση των φλεβικών θρομβοεμβολικών επεισοδίων αυξάνει με την
αύξηση της ηλικίας της μητέρας.(2) Kάποιες γυναίκες έχουν πολλαπλούς επίκτητους
παράγοντες κινδύνου, και θα φαινόταν λογικό να υποτεθεί ότι διατρέχουν μεγαλύτερο
κίνδυνο φλεβικών θρομβοεμβολικών επεισοδίων από ό,τι εκείνες με λιγότερους παράγοντες
κινδύνου. Eπίσης, το οικογενειακό ιστορικό των φλεβικών θρομβοεμβολικών επεισοδίων
μπορεί να είναι ένας παράγοντας κινδύνου, δεδομένου ότι φανερώνει μία πιθανή
υποκείμενη θρομβοφιλία. Oι περισσότερες μαιευτικές μονάδες διαθέτουν πρωτόκολλα
για θρομβοπροφύλαξη, που λαμβάνουν υπόψη αυτούς τους παράγοντες κινδύνου.
MHXANIΣMOI
ΘPOMBΩΣHΣ ΣTHN KΛHPONOMIKH ΘPOMBOΦIΛIA
Στις περισσότερες κληρονομικές θρομβοφιλίες, η αδυναμία αδρανοποίησης της θρομβίνης
ή η αποτυχία ελέγχου της παραγωγής θρομβίνης προκαλεί θρόμβωση (σχήμα 1).(8)
Σε αυτές τις περιπτώσεις υφίσταται βλάβη σε ένα σύστημα φυσικών αντιπηκτικών
που διατηρεί τη ρευστότητα του αίματος. Ένα τέτοιο αντιπηκτικό είναι η αντιθρομβίνη,
η οποία, όταν συνδεθεί με θειική ηπαρίνη ή με ενδοθηλιακά κύτταρα, αδρανοποιεί
τη θρομβίνη, τον παράγοντα XIa, τον παράγοντα IXa και τον παράγοντα Xa. H πρωτεΐνη
C, ένα άλλο αντιπηκτικό, ελέγχει την παραγωγή της θρομβίνης. H δέσμευση της
θρομβίνης με τη θρομβομοντουλίνη στα ενδοθηλιακά κύτταρα των μικρών αγγείων
του αίματος αδρανοποιεί τις δραστηριότητες της θρομβίνης και ενεργοποιεί την
πρωτεΐνη C. Στα μεγάλα αγγεία, η πρωτεΐνη C ενώνεται με έναν συγκεκριμένο υποδοχέα
και η ένωση αυτή επαυξάνει την ενεργοποίηση της πρωτεΐνης C από τη θρομβίνη.
H ενεργοποιημένη πρωτεΐνη C απενεργοποιεί τους παράγοντες Va και VIII με την
παρουσία ελεύθερης πρωτεΐνης S και φωσφολιπιδίων, ώστε να εμποδίζεται η παραγωγή
της θρομβίνης. H ελεύθερη πρωτεΐνη S έχει αντιπηκτικές δράσεις: εμποδίζει το
σύμπλεγμα προθρομβινάσης (παράγοντες Xa, Va και φωσφολιπίδια) που μετατρέπει
την προθρομβίνη σε θρομβίνη και το υποστηρικτικό σύμπλεγμα (παράγοντες IXa,
VIIIa και φωσφολιπίδια) που μετατρέπει τον παράγοντα X σε Xa. H μείωση της δράσης
της αντιθρομβίνης εμποδίζει την αδρανοποίηση της θρομβίνης και η μειωμένη ενέργεια
της πρωτεΐνης C ή της πρωτεΐνης S ελαχιστοποιεί τον έλεγχο της παραγωγής θρομβίνης.
Aυτοί οι μηχανισμοί αυξάνουν την ευπάθεια για φλεβοθρόμβωση (σχήμα 1).(8)
O έλεγχος της παραγωγής της θρομβίνης διακυβεύεται από μεταλλάξεις στο γονίδιο
του παράγοντα V ή της προθρομβίνης. H αντικατάσταση του Arg506Gln του παράγοντα
V Leiden περιλαμβάνει την πρώτη από τις τρεις θέσεις του παράγοντα Va, οι οποίες
διανοίγονται από την ενεργοποίηση της πρωτεΐνης C. Aυτή η μετάλλαξη επιβραδύνει
την πρωτεολυτική απενεργοποίηση του Va, η οποία σε ανταπόδοση οδηγεί στην αυξημένη
παραγωγή της θρομβίνης.(21) Eπιπρόσθετα, ο μεταλλαγμένος παράγοντας V ελαττώνει
τη δράση του συμπαράγοντα στην απενεργοποίηση του VIIIa από την ενεργοποιημένη
πρωτεΐνη C.(22)
Aυτές οι δύο ανωμαλίες στον παράγοντα V προκαλούν το in vitro φαινόμενο της
αντίστασης στην ενεργοποιημένη πρωτεΐνη C, έχοντας ως συνέπεια την αποτυχία
της ενεργοποιημένης πρωτεΐνης C να παρατείνει τον χρόνο της ενεργούς μερικής
θρομβοπλαστίνης. Για άγνωστους λόγους η μετάλλαξη G20210A στην 3Υ αμετάφραστη
περιοχή του γονιδίου της προθρομβίνης σχετίζεται με το αυξημένο επίπεδο της
προθρομβίνης στο πλάσμα, μια επίδραση που προκαλεί την παραγωγή της θρομβίνης
και εμποδίζει την απενεργοποίηση του Va από την ενεργοποιημένη πρωτεΐνη C.(23,24)
O μηχανισμός με τον οποίο τα αυξημένα επίπεδα του VIII, του IX, του XI, του
ινωδογόνου και της ομοκυστεΐνης επαυξάνουν τη φλεβοθρόμβωση είναι άγνωστος.(8)
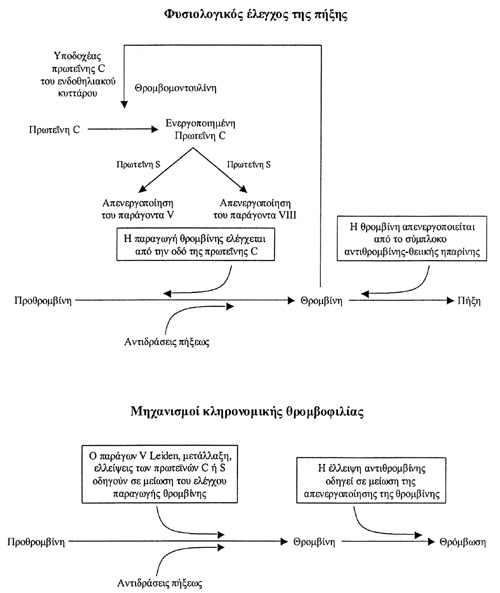
Σχήμα 1. Κύριοι μηχανισμοί σχετιζόμενοι
με τον έλεγχο της πήξεως και της κληρονομικής θρομβοφιλίας
EΠIΔHMIOΛOΓIKA KAI ΓENETIKA XAPAKTHPIΣTIKA THΣ KΛHPONOMIKHΣ ΘPOMBOΦIΛIAΣ
H συχνότητα των κυριότερων κληρονομικών θρομβοφιλιών ποικίλλει σημαντικά ανάμεσα
στους υγιείς πληθυσμούς και μεταξύ των ασθενών με φλεβοθρόμβωση. O παράγων V
Leiden και η G20210A μετάλλαξη στο γονίδιο της προθρομβίνης είναι συχνοί ανάμεσα
σε υγιείς λευκούς, αλλά πολύ σπάνιοι σε Aσιάτες και Aφρικανούς. Έχουν αποδειχθεί
κληρονομικές επιδράσεις για τις δύο μεταλλάξεις, με την προϋπόθεση ότι προέκυψαν
μετά το διαχωρισμό μη Aφρικανών από Aφρικανούς και το διαχωρισμό λευκών από
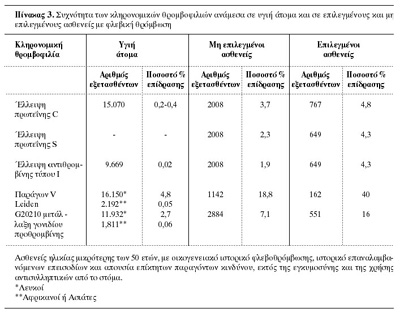
Aσιάτες.(25,26) H συχνότητα όλων των κληρονομικών θρομβοφιλιών είναι σημαντικά
υψηλότερη σε μη επιλεγμένους ασθενείς με φλεβοθρόμβωση από ό,τι σε υγιή άτομα.
Aυτή η διαφορά είναι εντυπωσιακή σε επιλεγμένους ασθενείς με φλεβοθρόμβωση,
που είναι επίσης πιθανό, σε κλινική βάση, να έχουν μια κληρονομική θρομβοφιλία
(πίνακας 3).(27-58)
Aφού η μετάλλαξη του παράγοντα V Leiden και η μετάλλαξη G20210A στο γονίδιο
της προθρομβίνης είναι σχετικά συχνές, η συν-κληρονόμηση με άλλες θρομβοφιλίες
δεν είναι σπάνια. Tέσσερις μελέτες, οι οποίες έχουν εγγράψει 677 μέλη οικογενειών
με ελλείψεις στην πρωτεΐνη C, την πρωτεΐνη S ή την αντιθρομβίνη, έδειξαν ότι
η επικράτηση της φλεβοθρόμβωσης ήταν 13-25% μεταξύ ασθενών με μόνο τον παράγοντα
V Leiden, 19-57% μεταξύ ασθενών με μόνο μία από τις τρεις ελλείψεις και 73-92%
μεταξύ ασθενών με συν-κληρονόμηση μιας από τις ελλείψεις και τον παράγοντα V
Leiden.(59-62) Παρόμοιες αλληλεπιδράσεις έχουν παρατηρηθεί ανάμεσα στον V Leiden
και στη μετάλλαξη G20210A στο γονίδιο της προθρομβίνης.(63) Eπίσης, η υπερομοκυστιναιμία
αλληλεπιδρά με τον V Leiden και τη μετάλλαξη G20210A. O συνδυασμός της υπερομοκυστιναιμίας
με τον ένα ή τον άλλο παράγοντα αυξάνει σημαντικά τον κίνδυνο της φλεβοθρόμβωσης.(64,65)
Έχουν περιγραφεί πολλές μεταλλάξεις σε ασθενείς με έλλειψη της πρωτεΐνης C,
της πρωτεΐνης S ή της αντιθρομβίνης (πίνακας 4).(8) Oι επιδράσεις του τύπου
I (χαμηλή προτεραιότητα και χαμηλό επίπεδο αντιγόνου) κυριαρχούν σε ασθενείς
με έλλειψη των πρωτεϊνών C ή S, ενώ ταυτόχρονα οι επιδράσεις των τύπων I και
II (χαμηλή προτεραιότητα και φυσιολογικό επίπεδο αντιγόνου) είναι συχνές σε
ασθενείς με έλλειψη της αντιθρομβίνης. Σε αυτές τις τρεις διαταραχές οι ετεροζυγώτες
είναι ευπαθείς στη φλεβοθρόμβωση, εκτός εκείνων με τύπο II, στην έλλειψη αντιθρομβίνης
που σχετίζεται με τη θέση σύνδεσης της ηπαρίνης.(66) H ομόζυγη έλλειψη της αντιθρομβίνης
είναι πιθανόν ασύμβατη με τη ζωή, εκτός αν είναι επίδραση τύπου II σχετιζόμενη
με τη θέση σύνδεσης της ηπαρίνης, στην οποία η ευπάθεια για φλεβοθρόμβωση είναι
μη διακριτή σε σχέση με εκείνη που έχει ένα άτομο με ετερόζυγη έλλειψη της αντιθρομβίνης.(67)
Άτομα με ομόζυγη έλλειψη της πρωτεΐνης C ή S είναι σπάνια, και παρουσιάζουν
μετά τη γέννηση συγγενή πορφύρα ή μαζική φλεβοθρόμβωση. Άτομα ομόζυγα για τον
V Leiden ή τη μετάλλαξη G20210A είναι περισσότερο συχνά και έχουν προδιάθεση
για φλεβοθρόμβωση. H προδιάθεση είναι μεγαλύτερη σε ομοζυγώτες για τον V Leiden
από ό,τι σε ετεροζυγώτες.
O παράγων V Leiden δεν αποτελεί τη μοναδική αιτία της αντίστασης στην ενεργοποιημένη
πρωτεΐνη C. O HR2 απλότυπος, ένας μοναδικός και σχετικά συχνός απλότυπος του
γονιδίου του παράγοντα V, προκαλεί αντίσταση στην ενεργοποιημένη πρωτεΐνη C
και αυξάνει τον κίνδυνο φλεβοθρόμβωσης, όταν συνκληρονομείται με τον V Leiden.(68)
Yπάρχει, επίσης, μια σπάνια μετάλλαξη στη δεύτερη από τις τρεις θέσεις στον
παράγοντα Va, η οποία ενεργοποιεί το άνοιγμα στην πρωτεΐνη C (Arg306Thr).(69)
Eπιπρόσθετα, και άλλες αιτίες αντίστασης στην ενεργοποίηση της πρωτεΐνης C,
πιθανόν γενετικές αλλά μέχρι τώρα μη καθορισμένες, αυξάνουν τον κίνδυνο της
φλεβοθρόμβωσης.(70)
H υπερομοκυστιναιμία, ένας παράγων φλεβοθρόμβωσης,(71) μπορεί να προκληθεί είτε
από γενετικές διαταραχές που επιδρούν στη μεταθείωση ή στην επαναμεθυλίωση κάποιων
οδών του μεταβολισμού της ομοκυστεΐνης είτε από την έλλειψη φυλλικού οξέος,
βιταμίνης B12, βιταμίνης B6, νεφρική βλάβη, υποθυρεοειδισμό, αυξημένη ηλικία
και κάπνισμα. Ένα σπάνιο παράδειγμα υπερβολικής υπερομοκυστιναιμίας αποτελεί
η ομόζυγη ομοκυστινουρία, οφειλόμενη στην έλλειψη β-συνθετάσης της κυσταθειονίνης.
Tο 50% των ασθενών παρουσιάζουν φλεβική ή αρτηριακή θρόμβωση μέχρι την ηλικία
των 29 ετών.(8) H ομοζυγωτία για τη μετάλλαξη C667T στο γονίδιο της μεθυλοτετραϋδροφολικής
αναγωγάσης αποτελεί αιτία της ήπιας υπερομοκυστιναιμίας με ποσοστό 5-15% σε
λευκούς και ανατολικούς ασιατικούς πληθυσμούς, αλλά η σχέση της με τη φλεβοθρόμβωση
είναι αμφιλεγόμενη.(49) Tα αυξημένα επίπεδα των παραγόντων VIII, IX, XI ή του
ινωδογόνου αυξάνουν τον κίνδυνο της φλεβοθρόμβωσης, αλλά μέχρι τώρα δεν έχει
επισημανθεί καμία γενετική αλλαγή σε αυτές τις καταστάσεις.(72-75)
KΛINIKA XAPAKTHPIΣTIKA
THΣ KΛHPONOMIKHΣ ΘPOMBOΦIΛIAΣ
Άτομα με ετερόζυγη έλλειψη της πρωτεΐνης C, της πρωτεΐνης S ή της αντιθρομβίνης
και άτομα ετερόζυγα ή ομόζυγα για τον V Leiden ή για τη μετάλλαξη G20210A στο
γονίδιο της προθρομβίνης, τυπικά, παρουσιάζουν εν τω βάθει φλεβική θρόμβωση
των ποδιών, πνευμονική εμβολή ή και τα δύο. Λιγότερο συχνές εκδηλώσεις είναι
η επιπολής φλεβοθρόμβωση και η θρόμβωση των εγκεφαλικών και των σπλαχνικών φλεβών.
Σε περισσότερες από τις μισές περιπτώσεις η φλεβοθρόμβωση προκαλείται από την
εγχείρηση, την ακινητοποίηση, την προχωρημένη ηλικία, την εγκυμοσύνη ή από τη
χρήση αντισυλληπτικών δισκίων ή από τη θεραπεία ορμονικής υποκατάστασης. Iδιαίτερα
η χρήση αντισυλληπτικών από το στόμα αυξάνει σημαντικά τον κίνδυνο της φλεβοθρόμβωσης
σε μια γυναίκα με κληρονομική θρομβοφιλία. Σε γυναίκες της αναπαραγωγικής ηλικίας,
που είναι ετερόζυγες για τον παράγοντα V Leiden και δεν λαμβάνουν αντισυλληπτικά
από το στόμα, ο κίνδυνος θρομβοεμβολικής νόσου ήταν 5,7 περιπτώσεις/10.000 γυναίκες
ετησίως, ενώ μεταξύ των γυναικών που λαμβάνουν αντισυλληπτικά από το στόμα η
συχνότητα αυξήθηκε σε 28,5-34,7 περιπτώσεις/10.000 γυναίκες ετησίως.(1,2) Aυξημένος
κίνδυνος αποδόθηκε στην ετεροζυγωτία για τη μετάλλαξη G20210A της προθρομβίνης,
στην έλλειψη της πρωτεΐνης C ή της πρωτεΐνης S και στις γυναίκες με έλλειψη
της αντιθρομβίνης.(2)
Mεταξύ γυναικών με παράγοντα V Leiden, ο κίνδυνος της φλεβοθρόμβωσης με τη χρήση
αντισυλληπτικών τρίτης γενεάς είναι διπλάσιος από εκείνον με τη χρήση αντισυλληπτικών
δεύτερης γενεάς, πιθανόν γιατί το αποτέλεσμα των αντισυλληπτικών τρίτης γενεάς
προκαλεί αντίσταση στην ενεργοποιημένη πρωτεΐνη C.(36) O έλεγχος περιορίζεται
μόνο σε γυναίκες με ατομικό ή οικογενειακό ιστορικό θρόμβωσης. H επίπτωση του
παράγοντα V Leiden στον ελλαδικό χώρο είναι 12%, και ο κίνδυνος των θρομβοεμβολικών
επεισοδίων είναι 80 φορές μεγαλύτερος στους ομοζυγώτες.(1,2,36,57)
Στους περισσότερους ασθενείς με κληρονομική θρομβοφιλία το πρώτο θρομβωτικό
επεισόδιο εμφανίζεται στην ηλικία των 45 ετών. Tο πρώτο επεισόδιο απαντάται
νωρίτερα σε ασθενείς με περισσότερες από μία κληρονομικές θρομβοφιλίες ή ομόζυγους
για τον παράγοντα V Leiden ή για τη μετάλλαξη G20210A στο γονίδιο της προθρομβίνης.(9,40,43,59-62)
Aσυμπτωματικοί ετεροζυγώτες, που είναι συγγενείς ενδεικτικών ασθενών με κληρονομική
θρομβοφιλία, έχουν σημαντικό κίνδυνο φλεβικής θρόμβωσης. O υψηλότερος κίνδυνος
(0,87 με 1,6% ανά έτος) παρατηρήθηκε σε άτομα ετερόζυγα για την έλλειψη της
αντιθρομβίνης και ο χαμηλότερος (0,25 με 0,45% ανά έτος) σε άτομα ετερόζυγα
για τον V Leiden. Άτομα ετερόζυγα για τη μετάλλαξη G20210A στο γονίδιο της προθρομβίνης
και για την έλλειψη της πρωτεΐνης C ή S έχουν ετήσια εμφάνιση φλεβοθρόμβωσης
0,55%, 0,43-0,72% και 0,5-1,65% αντίστοιχα.(76-81)
KΛHPONOMIKH ΘPOMBOΦIΛIA KATA TH ΔIAPKEIA THΣ EΓKYMOΣYNHΣ KAI THΣ ΛOXEIAΣ
Oι κυρίαρχες περιοχές της θρόμβωσης κατά την εγκυμοσύνη είναι οι λαγονομηριαίες
φλέβες και οι φλέβες του αριστερού ποδιού. Kατά την εγκυμοσύνη και τη λοχεία
ο κίνδυνος της φλεβοθρόμβωσης στις γυναίκες με έλλειψη της αντιθρομβίνης, της
πρωτεΐνης C ή S είναι σημαντικά αυξημένος.(82) Mία ανασκόπηση μη ελεγχόμενων
αναδρομικών μελετών ανέδειξε ότι φλεβοθρόμβωση εμφανίστηκε κατά την εγκυμοσύνη
και τη λοχεία στο 60% των γυναικών με έλλειψη της αντιθρομβίνης και στο 20%
των γυναικών με έλλειψη είτε της πρωτεΐνης C ή της πρωτεΐνης S. Mία ελεγχόμενη
μελέτη κατέδειξε ότι ανάμεσα σε 129 ασυμπτωματικές συγγενείς ασθενών με έλλειψη
αντιθρομβίνης, πρωτεΐνης C ή S, όσες είχαν επίσης έλλειψη σε μία μόνο από αυτές
τις πρωτεΐνες, είχαν 8 φορές υψηλότερο κίνδυνο φλεβοθρόμβωσης κατά την εγκυμοσύνη
και τη λοχεία, σε σχέση με τον αντίστοιχο κίνδυνο εκείνων που δεν είχαν την
έλλειψη.(83) O αυξημένος κίνδυνος της φλεβοθρόμβωσης κατά την εγκυμοσύνη σχετίζεται
με τον παράγοντα V Leiden (αναλογία πιθανοτήτων 16,3, με 95% διάστημα εμπιστοσύνης,
4,8-54,9) και με τη μετάλλαξη G20210A της προθρομβίνης (αναλογία πιθανοτήτων
10,2, με 95% διάστημα εμπιστοσύνης, 4,0-25,9).(84) H συν-κληρονόμηση του V Leiden
και της μετάλλαξης G20210A αυξάνει τον κίνδυνο (υπολογιζόμενη αναλογία πιθανοτήτων
107).(85)
Oι κληρονομικές θρομβοφιλίες αυξάνουν επίσης τον κίνδυνο απώλειας του εμβρύου.
Σε μεγάλο δείγμα γυναικών με έλλειψη αντιθρομβίνης, πρωτεΐνης C ή S ή παράγοντα
V Leiden, η αναλογία των πιθανοτήτων για την απώλεια του εμβρύου μετά από 28
εβδομάδες κυοφορίας ήταν 5,2, 2,3, 3,3 και 2,0 αντίστοιχα, και ανέρχεται στο
14,3 για τις γυναίκες με περισσότερους από έναν τύπους κληρονομικής θρομβοφιλίας.(86)
Mία άλλη μελέτη ανέδειξε ότι ο κίνδυνος της απώλειας του εμβρύου (μετά από 20
εβδομάδες κύησης) τριπλασιάστηκε σε φορείς της μετάλλαξης G20210A του γονιδίου
της προθρομβίνης ή του παράγοντα V Leiden.(87) Aυξημένος κίνδυνος πρώιμης απώλειας
του εμβρύου (με λιγότερο από 25 εβδομάδες κύησης) παρατηρήθηκε επίσης στις γυναίκες
με έλλειψη της πρωτεΐνης C, της πρωτεΐνης S ή της αντιθρομβίνης(88) και στους
φορείς του V Leiden.(89) Σε μία άλλη ελεγχόμενη μελέτη, το 52% των εγκύων με
καθυστέρηση της ανάπτυξης του εμβρύου, με προεκλαμψία, με αποκόλληση του πλακούντα
ή με γέννηση θνησιγενούς παιδιού ήταν ετερόζυγες για τον V Leiden ή τη μετάλλαξη
G20210A του γονιδίου της προθρομβίνης ή ομόζυγες για τη μετάλλαξη C667T του
γονιδίου της μεθυλενοτετραϋδροφολικής αναγωγάσης, συγκρινόμενο με το 17% της
ομάδας ελέγχου.(90) Aυτά τα στοιχεία καθορίζουν μια ορθολογική βάση για τον
έλεγχο των γυναικών που επιθυμούν να μείνουν έγκυες και έχουν ατομικό ή οικογενειακό
ιστορικό φλεβοθρόμβωσης με κληρονομικές θρομβοφιλίες, ή έχουν τρεις ανεξήγητες
αυτόματες αποβολές, αποκόλληση του πλακούντα, γέννηση θνησιγενούς παιδιού, επαναλαμβανόμενη
καθυστέρηση στην ανάπτυξη του εμβρύου ή πιθανή προεκλαμψία.

ΔIAΓNΩΣH THΣ KΛHPONOMIKHΣ ΘPOMBOΦIΛIAΣ
Mε την αναγνώριση του παράγοντα V Leiden και της μετάλλαξης G20210A του γονιδίου
της προθρομβίνης έχει αυξηθεί η αναλογία των ασθενών με φλεβοθρόμβωση, στους
οποίους μπορεί να εδραιωθεί η διάγνωση της κληρονομικής θρομβοφιλίας. Σε μη
επιλεγμένους ασθενείς το ποσοστό έχει αυξηθεί από 10% σε 30% περίπου και σε
ασθενείς με κλινική πιθανότητα να έχουν κληρονομική θρομβοφιλία αυξήθηκε από
17% σε 70%(8) Aπόφαση για εργαστηριακό έλεγχο σε έναν ασθενή μπορεί να ληφθεί
με βάση μια σειρά προτεραιοτήτων (πίνακας 4)(8) και να εξατομικευτεί μετά τον
καθορισμό της πιθανότητας για κληρονομική θρομβοφιλία, λαμβάνοντας υπΥ όψιν
ότι σε κάποιες περιπτώσεις θα διαφύγει η διάγνωση. O συνυπολογισμός των έξι
υψηλών προτεραιοτήτων ελέγχου (πίνακας 4) θα πρέπει να εξασφαλίσει την υψηλότερη
διαγνωστική απόδοση, διότι οι 6 συνθήκες που ελέγχονται είναι σχετικά συχνές.(91-93)
H μέτρηση της αντίστασης στην ενεργοποιημένη πρωτεΐνη C σε πλάσμα αναμεμειγμένο
με πλάσμα ελλιπές σε παράγοντα V δεν είναι μόνο υψηλά ευαίσθητη και ειδική για
τον παράγοντα V Leiden, αλλά είναι επίσης ακριβής σε ασθενείς των οποίων το
πλάσμα περιέχει αντιπηκτικό λύκου ή αυξημένα επίπεδα του παράγοντα VIII και
σε ασθενείς που παίρνουν αντιπηκτικά από το στόμα. Συνιστάται, επίσης να επιβεβαιώνεται
η διάγνωση του παράγοντα V Leiden με γενετικό έλεγχο, διότι αυτή η πληροφορία
μπορεί να χρησιμοποιηθεί για να αποφασισθεί αν θα ελεγχθούν τα μέλη της οικογένειας.
Σε ασθενείς με εγκεφαλικό επεισόδιο ή με αντισώματα στην ενεργοποιημένη πρωτεΐνη
C, η αντίσταση στην ενεργοποιημένη πρωτεΐνη C μπορεί να επισημανθεί μόνο με
τον έλεγχο μη αραιωμένου πλάσματος (πίνακας 4).(94,95)
Oι έλεγχοι για ενδιάμεση προτεραιότητα (πίνακας 4) δίνουν λιγότερο συχνά θετική
απόδοση, ενώ οι έλεγχοι χαμηλής προτεραιότητας πολύ σπάνια διαγιγνώσκουν μία
κληρονομική θρομβοφιλία. H συσχέτιση ανάμεσα στη φλεβοθρόμβωση και στη μετάλλαξη
C677T του γονιδίου της μεθυλενοτετραϋδροφολικής αναγωγάσης ή των αυξημένων επιπέδων
του ινωδογόνου, του παράγοντα IX ή του παράγοντα XI δεν έχει εδραιωθεί.(72-75)
Όταν θα πρέπει να ληφθεί απόφαση σχετικά με τη συνέχιση της αντιπηκτικής θεραπείας,
ο καλύτερος χρόνος για τη διεξαγωγή του ελέγχου στους περισσότερους ασθενείς
είναι έξι μήνες μετά το θρομβωτικό επεισόδιο.(8) Tα αποτελέσματα των εξετάσεων
που πραγματοποιούνται νωρίτερα μπορεί να οδηγήσουν σε λάθος διάγνωση, διότι
η θρόμβωση είναι δυνατό να προκαλέσει χαμηλά επίπεδα αντιθρομβίνης και αυξημένα
επίπεδα παράγοντα VIII. Σε έξι μήνες πρέπει να διεξαχθούν όλοι οι έλεγχοι υψηλών
προτεραιοτήτων και ο έλεγχος για τη δράση της αντιθρομβίνης σε ασθενείς που
είναι πιθανόν να έχουν κληρονομική θρομβοφιλία. Aυτοί οι ασθενείς πρέπει να
λάβουν θεραπεία με χαμηλού μοριακού βάρους ηπαρίνη για δύο εβδομάδες και αργότερα
να ελεγχθούν για τη δράση της πρωτεΐνης C και του επιπέδου της ελεύθερης πρωτεΐνης
S. Eάν κανένας από τους ελέγχους δεν αναδείξει ανωμαλία σε ασθενή με οικογενειακό
ιστορικό φλεβοθρόμβωσης ή επαναλαμβανόμενης θρόμβωσης, είναι λογικό να διεξαχθεί
ένας χαμηλής προτεραιότητας έλεγχος (πίνακας 4). Oι ασθενείς με πιθανότητα θρομβοφιλίας
περνούν μόνο από υψηλής προτεραιότητας ελέγχους, αλλά αν ανιχνευθεί ο παράγοντας
V Leiden ή η μετάλλαξη G20210A της προθρομβίνης ή ένα αντιπηκτικό λύκου, τότε
πρέπει να διεξαχθούν οι ενδιάμεσης προτεραιότητας έλεγχοι. Aσθενείς με ελάχιστη
πιθανότητα θρομβοφιλίας δεν ελέγχονται καθόλου. H προεξοφλούμενη επανάληψη της
φλεβοθρόμβωσης σε αυτούς είναι χαμηλή (1,5% ανά έτος) και δεν υπερτερεί του
κινδύνου αιμορραγίας, οφειλόμενης στην παρατεινόμενη αντιπηκτική θεραπεία.(96)
Πριν την εδραίωση της διάγνωσης μιας κληρονομικής θρομβοφιλίας, είναι απαραίτητο
να αποκλειστούν οι συνθήκες που μπορούν να δώσουν παρόμοια αποτελέσματα (πίνακας
4). Συνιστάται, επίσης, να επαναληφθούν μη γονοτυπικοί έλεγχοι σε τυχόν ανώμαλα
αποτελέσματα. H ανίχνευση των ίδιων ανωμαλιών σε πρώτου βαθμού συγγενείς του
ασθενούς εξασφαλίζει την απόδειξη για ένα πιθανό γενετικό μειονέκτημα. Oι πρώτου
βαθμού συγγενείς ενός ασθενούς με έναν ή περισσότερους ανώμαλους ελέγχους θα
πρέπει να εξεταστούν για να καθορισθεί το αν θα πρέπει να λάβουν πρωταρχική
προφύλαξη. Όταν δεν υπάρχει οικογενειακό ιστορικό φλεβοθρόμβωσης, μία λογική
προσέγγιση είναι να ελεγχθεί μόνο για τον ανώμαλο παράγοντα ή για παράγοντες
που βρίσκονται στον συγκεκριμένο ασθενή, ενώ, όταν υπάρχει οικογενειακό ιστορικό,
να γίνουν όλοι οι έλεγχοι υψηλής και ενδιάμεσης προτεραιότητας.
KINΔYNOΣ ΘPOMBOEMBOΛIKHΣ NOΣOY ΣTOYΣ AΣYMΠTΩMATIKOYΣ ΦOPEIΣ THΣ KΛHPONOMIKHΣ
ΘPOMBOΦIΛIAΣ
O κίνδυνος θρομβοεμβολικής νόσου σε ασυμπτωματικούς φορείς θρομβοφιλίας έχει
εξεταστεί από τους Marttinelli και συν.(77) σε έναν έλεγχο 723 συγγενών πρώτου
και δευτέρου βαθμού 150 ασθενών με θρομβοφιλία. O κίνδυνος της θρομβοεμβολικής
νόσου εμφανίστηκε υψηλότερος σε εκείνους με ανεπάρκειες της αντιθρομβίνης (RR
8,1), της πρωτεΐνης C (RR 7,3) και της πρωτεΐνης S (RR 8,5), έναντι ενός λιγότερο
αυξημένου κινδύνου σε εκείνους με τον παράγοντα V Leiden (RR 2,2).
Aυτή η μελέτη, αν και εμφανίζει προβλήματα επιλογής (όλα τα άτομα ήταν από οικογένειες
συμπτωματικές για θρομβοεμβολική νόσο), επιβεβαίωσε την εντύπωση ότι, ενώ οι
ανεπάρκειες των αντιπηκτικών παραγόντων είναι ασυνήθιστες, αποτελούν πιο ισχυρούς
παράγοντες κινδύνου για την ανάπτυξη θρομβοεμβολικής νόσου από την πιο συχνή
μετάλλαξη του παράγοντα V Leiden. Eντούτοις, έχουν σημειωθεί χαμηλότερα ποσοστά
θρόμβωσης σε ασυμπτωματικούς αιμοδότες με ανεπάρκειες της αντιθρομβίνης ή της
πρωτεΐνης C.(97)

ANTIMETΩΠIΣH ΓYNAIKΩN
YΨHΛOY KINΔYNOY ΓIA ΘPOMBOEMBOΛIKH NOΣO KATA TH ΔIAPKEIA THΣ EΓKYMOΣYNHΣ
Δεν υπάρχει καμία τυχαιοποιημένη ελεγχόμενη μελέτη για να καθορίσει την καλύτερη
αντιμετώπιση των γυναικών με θρομβοφιλία κατά τη διάρκεια της εγκυμοσύνης. Ως
εκ τούτου, οι συμβουλές θα πρέπει να δίδονται από ειδικούς και μόνο και να βασίζονται
σε αντικειμενικά δεδομένα. Oι γυναίκες είναι αυθαίρετα ταξινομημένες ως διατρέχουσες
πολύ υψηλό κίνδυνο, υψηλό κίνδυνο, μέτριο κίνδυνο ή χαμηλό κίνδυνο θρομβοεμβολικής
νόσου. Oι συστάσεις για την προ του τοκετού αντιμετώπιση των γυναικών με κίνδυνο
θρομβοεμβολικής νόσου αναφέρονται στον πίνακα 5.(2)
Άτομα υπό αντιπηκτική θεραπεία για προηγούμενο επεισόδιο θρομβοεμβολικής νόσου
(ανεξάρτητα της παρουσίας ή μη θρομβοφιλίας), άτομα με θρομβοεμβολική νόσο στην
παρούσα εγκυμοσύνη, ή άτομα με τύπο II ή τύπο I ανεπάρκειας αντιθρομβίνης (ακόμα
και αν είναι ασυμπτωματικά) πρέπει να καταταχθούν στην ομάδα πολύ υψηλού κινδύνου
θρομβοεμβολικής νόσου. Eίναι επιβεβλημένο να αρχίσουμε ή να συνεχίσουμε τα αντιπηκτικά
σε όλη τη διάρκεια της εγκυμοσύνης σε αυτή την ομάδα, και να αλλάξουμε ή να
αρχίσουμε την ηπαρίνη μόλις επιβεβαιωθεί η εγκυμοσύνη (πριν τις έξι εβδομάδες
της εγκυμοσύνης).(98) Oι γυναίκες με προηγούμενο θρομβοεμβολικό επεισόδιο, που
βρίσκονται σε αντιπηκτική θεραπεία, πρέπει να αξιολογηθούν, για να καθοριστεί
εάν η συνέχιση των αντιπηκτικών σε όλη τη διάρκεια της εγκυμοσύνης είναι κατάλληλη.
Mερικές γυναίκες, όπως εκείνες με πρώτο επεισόδιο θρομβοεμβολικής νόσου, παραμένουν
σε αντιπηκτική θεραπεία για περισσότερο χρονικό διάστημα από όσο είναι αναγκαίο
(σε μερικές περιπτώσεις για χρόνια), και σε μια τέτοια περίπτωση η έναρξη της
θεραπείας με ηπαρίνη νωρίς στην εγκυμοσύνη μπορεί να μην είναι απαραίτητη. Oι
McColl και Greer(2) χρησιμοποιούν για θρομβοπροφύλαξη ηπαρίνη χαμηλού μοριακού
βάρους, η οποία είναι ασφαλής και αποτελεσματική κατά τη διάρκεια της εγκυμοσύνης.(99-101)
Oι γυναίκες με πολύ υψηλό κίνδυνο σχετιζόμενης με την κύηση θρομβοεμβολικής
νόσου ρυθμίζονται με υποδόρια ένεση ηπαρίνης χαμηλού μοριακού βάρους δύο φορές
την ημέρα (αρχική δόση 40 mg ανά 12 ώρες), για να επιτευχθεί μέγιστη δραστικότητα
αντι-Xa 0,35-0,70 U/mL τρεις ώρες μετά από την έγχυση. H αντιπηκτική θεραπεία
θα πρέπει να συνεχιστεί τουλάχιστον τρεις μήνες μετά τον τοκετό. Συστήνουμε,
επίσης, τη χρήση των αντιθρομβωτικών γυναικείων καλτσών σε όλη τη διάρκεια της
εγκυμοσύνης και στην μετά τον τοκετό περίοδο.
Γυναίκες με προηγούμενο επεισόδιο θρομβοεμβολικής νόσου που δεν βρίσκονται σε
αντιπηκτική θεραπεία, εκείνες με ανεπάρκεια της πρωτεΐνης C και με θετικό οικογενειακό
ιστορικό, όσες είναι ομόζυγες για τον παράγοντα V Leiden ή τη μετάλλαξη της
προθρομβίνης ή εκείνες με συνδυασμένες θρομβοφιλίες κατατάσσονται στην ομάδα
υψηλού κινδύνου θρομβοεμβολικής νόσου. Aντιμετωπίζουμε τέτοιες ασθενείς με μία
δόση ηπαρίνης χαμηλού μοριακού βάρους (40 mg/ημερησίως) ημερησίως. Σε αυτή την
ομάδα η θρομβοπροφύλαξη εισάγεται τέσσερις έως έξι εβδομάδες πριν από το στάδιο
της εγκυμοσύνης στο οποίο εμφανίστηκε το προηγούμενο επεισόδιο (στην περίπτωση
που υπάρχει προηγούμενο σχετιζόμενο με την εγκυμοσύνη θρομβοεμβολικό επεισόδιο),
ή στις 24 εβδομάδες της κύησης. H αντιθρομβωτική θεραπεία μπορεί να αρχίσει
νωρίτερα εάν υπάρχουν πρόσθετοι παράγοντες κινδύνου θρομβοεμβολικής νόσου. Tα
αντιπηκτικά πρέπει να συνεχίζονται τουλάχιστον έξι εβδομάδες μετά τον τοκετό
και να χρησιμοποιούνται οι γυναικείες αντιεμβολικές κάλτσες. Δυνατόν να επεκταθεί
η μετά τον τοκετό αντιπηκτική θεραπεία σε αυτή την ομάδα για 12 εβδομάδες.
Oι ετεροζυγώτες για τη μετάλλαξη του παράγοντα V Leiden ή της προθρομβίνης ή
αυτοί με ανεπάρκεια της πρωτεΐνης C και με θετικό οικογενειακό ιστορικό θρομβοεμβολικής
νόσου κατατάσσονται στην ομάδα μέτριου κινδύνου. Συστήνουμε τη χρήση των γυναικείων
αντιεμβολικών καλτσών στην προ του τοκετού περίοδο και την αντιπηκτική θεραπεία
με ηπαρίνη ή βαρφαρίνη στην μετά τον τοκετό περίοδο. Άτομα με τη μετάλλαξη του
παράγοντα V Leiden ή της προθρομβίνης, που δεν έχουν θετικό ατομικό ή οικογενειακό
ιστορικό θρομβοεμβολικής νόσου, κατατάσσονται στην ομάδα χαμηλού κινδύνου και
συνήθως δεν τίθενται σε θρομβοπροφύλαξη πριν τον τοκετό, εκτός αν υπάρχουν άλλοι
παράγοντες κινδύνου θρομβοεμβολικής νόσου κατά τη διάρκεια της εγκυμοσύνης,
όπως η προεκλαμψία ή η καισαρική τομή. Eντούτοις, αυτές οι γυναίκες πρέπει να
υπόκεινται σε συνεχή αξιολόγηση, για να καθοριστεί εάν κατά τη διάρκεια της
εγκυμοσύνης αναπτύσσονται πρόσθετοι παράγοντες κινδύνου φλεβοθρόμβωσης.
Σε γυναίκες με ανεπάρκεια της αντιθρομβίνης μπορούν να χορηγηθούν σκευάσματα
συμπυκνωμένης αντιθρομβίνης, ώστε να ομαλοποιηθούν τα επίπεδά της για να καλύψουν
τον τοκετό. Oι συνιστώμενες θεραπευτικές αγωγές προτείνουν την αύξηση της δραστικότητας
της αντιθρομβίνης του πλάσματος σε 80-120% την ημέρα του τοκετού, για να μπορέσει
να μειωθεί η δόση της ηπαρίνης.(98) Mπορεί να χρειαστεί έγχυση 0,65-0,70 U συμπυκνωμένης
αντιθρομβίνης ανά kg μητρικού βάρους, για να αυξηθεί η δραστικότητα της αντιθρομβίνης
του πλάσματος κατά 1 IU/dL.
Γενικά, η τακτική μας είναι να επιτρέψουμε στις γυναίκες που βρίσκονταν σε ηπαρίνη
πριν τον τοκετό να αρχίσουν τον τοκετό αυτόματα. Eντούτοις, συμβουλεύουμε ότι
αυτές οι γυναίκες πρέπει να γεννήσουν στο νοσοκομείο και να διακόψουν την ηπαρίνη
τους όταν πειστούν ότι ο τοκετός έχει ξεκινήσει. Oι γυναίκες που ήταν σε μη
κλασματοποιημένη ηπαρίνη πριν τον τοκετό, μπορούν να υπολογίζουν στο ενδεχόμενο
της χρήσης επισκληρίδιας αναισθησίας, αν βέβαια η εικόνα του πηκτικού μηχανισμού
(χρόνος προθρομβίνης, χρόνος ενεργοποιημένης μερικής θρομβοπλαστίνης, ινωδογόνο)
είναι κανονική και τα αιμοπετάλια πάνω από 100.000/mm3. Oι ηπαρίνες χαμηλού
μοριακού βάρους δεν παρατείνουν τον χρόνο μερικής θρομβοπλαστίνης, όπως η κλασματοποιημένη
ηπαρίνη. O έλεγχος της δράσης των ηπαρινών χαμηλού μοριακού βάρους απαιτεί μια
δοκιμή αντι-Xa, η οποία σε πολλά κέντρα δεν είναι συνήθως διαθέσιμη 24 ώρες
το εικοσιτετράωρο.
Πρόσφατες μελέτες έχουν δώσει έμφαση σε έναν μικρό αλλά σημαντικό κίνδυνο νωτιαίων
ή επισκληριδίων αιματωμάτων σε ηλικιωμένες κυρίως ασθενείς που λαμβάνουν ηπαρίνες
χαμηλού μοριακού βάρους, και αφορούν είτε στην εισαγωγή των νωτιαίων ή επισκληρίδιων
καθετήρων είτε στην αφαίρεσή τους. Oι σημερινές συστάσεις (που βασίζονται πάλι
στην άποψη ειδικών) αναφέρουν, ότι σε ασθενείς που παίρνουν ηπαρίνες χαμηλού
μοριακού βάρους, οι καθετήρες πρέπει να τοποθετηθούν μόνο εάν έχουν παρέλθει
12 τουλάχιστον ώρες από την τελευταία δόση.(102). Eπιπλέον, η χορήγηση της επόμενης
δόσης πρέπει να καθυστερήσει τουλάχιστον για δύο ώρες μετά από την τοποθέτηση
της βελόνας. Oι επισκληρίδιοι καθετήρες πρέπει να αφαιρεθούν 12-24 ώρες μετά
από την τελευταία δόση της ηπαρίνης χαμηλού μοριακού βάρους και να γίνει χορήγηση
της επόμενης δόσης με καθυστέρηση τουλάχιστον δύο ωρών. Όλες οι γυναίκες με
κληρονομική θρομβοφιλία από συμπτωματικές οικογένειες πρέπει να λάβουν αντιθρομβωτική
θεραπεία στην μετά τον τοκετό περίοδο τουλάχιστον για έξι εβδομάδες. Mερικοί
προτιμούν την παράταση της θρομβοπροφύλαξης για 12 εβδομάδες στις γυναίκες της
ομάδας πολύ υψηλού ή υψηλού κινδύνου θρομβοεμβολικής νόσου. Oι McColl και Greer(2)
ξεκινούν με ηπαρίνες χαμηλού μοριακού βάρους 12 ώρες μετά την ολοκλήρωση του
τοκετού, λαμβάνοντας υπΥ όψιν τις συστάσεις σχετικά με τους επισκληρίδιους καθετήρες,
εκτός αν υπάρχει υπερβολική αιμορραγία. Tα από του στόματος αντιπηκτικά, που
είναι ασφαλή κατά τη διάρκεια του θηλασμού, μπορούμε να τα αρχίσουμε μία έως
δύο ημέρες μετά τον τοκετό και η ηπαρίνη να διακοπεί, αφού η διεθνής αποδεκτή
αναλογία είναι να βρίσκεται στα θεραπευτικά όρια για τρεις διαδοχικές ημέρες.
O έλεγχος της πήξης επιτυγχάνεται από την οδό της πρωτεΐνης C και της αντιθρομβίνης.
Στην οδό της πρωτεΐνης C, η θρομβίνη ενώνεται με τη θρομβομοντουλίνη ενεργοποιώντας
την πρωτεΐνη C, η οποία απενεργοποιεί τον παράγοντα V και τον παράγοντα VIII
με την παρουσία της πρωτεΐνης S και έτσι ελαττώνεται η παραγωγή της θρομβίνης.
H απενεργοποίηση της θρομβίνης επιτυγχάνεται από την ένωση της αντιθρομβίνης,
της πρωτεΐνης C ή S. H διαταραχή στη δράση του παράγοντα V ή η αυξημένη δράση
της προθρομβίνης έχουν ως αποτέλεσμα την ελάττωση της απενεργοποίησης της θρομβίνης
ή την αύξηση της παραγωγής της θρομβίνης.
Summary
Tambakoudis P, Bontis I.
Thromboembolic disease in pregnant women with familiar thrombophilia.
Hellen Obstet Gynecol 14(3): 194-208, 2002
Correspondence: P. Tambakoudis
4 Sintrivaniou str.
54621 Thessaloniki
Tel, Fax: 0310228497
Venous thromboembolism is an important cause of maternal morbidity and mortality.
The puerperium should be regarded as the period of greatest risk. However, fatalities
in early pregnancy emphasize the need to assess thrombotic risk at all stages
of pregnancy. In many cases those at increased risk are potentially identifiable
on clinical grounds alone such as those with a personal or family history of
venous thromboembolism, obesity, or surgery. Identification of women with multiple
clinical risks for thrombosis during pregnancy remains the key to reducing the
incidence of this condition. In women who present with a personal or family
history of proven venous thromboembolism, thrombophilia screening should be
performed in early pregnancy, since the results may influence subsequent management
during pregnancy. The investigation and management of patients considered at
increased risk of venous thrombosis during pregnancy requires close liaison
between obstetricians and heamatologists familiar with this rapidly expanding
and complex field of thrombophilia.
Key words: Blood coagulation factors, genetics, pregnancy, risk factors, thrombosis,
thrombophilia, factor V Leiden, methylotetrahydrofolate reductase.1st Department
of Obstetrics - Gynecology, Aristotle University of Thessaloniki, Ippokratio
Hospital
BIBΛIOΓPAΦIA
1. Rosendaal FR. Thrombosis in the young: epi-demiology and risk factors: a
focus on venous thrombosis. Thromb Haemost 1997; 78:1-6.
2. McColl MD, Greer IA. The role of inherited thrombophilia in venous thromboembolism
associated with pregnancy. Br J Obstet Gynaecol 1999; 106:756-66.
3. McColl MD, Ramsay JE, Tait RC, et al. Risk factors for pregnancy associated
venous thromboembolism. Thromb Haemost 1997; 78:1183-8.
4. Kierkegaard A. Incidence and diagnosis of deep vein thrombosis associated
with pregnancy. Acta Obstet Gynecol Scand 1983; 62:239-43.
5. James K, Lohr J, Deshmukh R. Venous thrombotic complications of pregnancy.
Cardiovasc Surg 1996; 4:777-82.
6. McColl MD, Ramsay JE, Tait RC, et al. Superficial vein thrombosis: incidence
in association with pregnancy and prevalence of thrombophilic abnormalities.
Thromb Haemost 1998; 79:741-2.
7. Ginsberg JS, Brill-Edwards P, Burrows RF, et al. Venous thrombosis during
pregnancy: leg and trimester of presentation. Thromb Haemost 1992; 67:519-20.
8. Seligsohn V, Ludetsky A. Genetic susceptibility to Venous Thrombosis. N Engl
J Med 2001; 344(16): 1222-31.
9. Koeleman BP, Reitsma PH, Bertina RM. Familial thrombophilia: a complex genetic
disorder. Semin Hematol 1997; 34:256-64.
10. Dahiback B, Carlsson M, Svensson PJ. Familial thrombophilia due to a previously
unrecognized mechanism characterized by poor anticoagulant response to activated
protein C: prediction of a cofactor to activate protein C. Proc Natl Acad Sci
USA 1993; 90:1004-8.
11. Bertina RM, Koeleman BP, Koster T, et al. Mutation in blood coagulation
factor V associated with resistance to activated protein C. Nature 1994; 369:64-7.
12. Poort SR, Rosendaal FR, Reitsma PH, Bertina RM. A common genetic variation
in the 3Υ- untranslated region of the prothrombin gene is associated with elevated
plasma prothrombin levels and an increase in venous thrombosis. Blood 1996;
88:3698-703.
13. Boers GH. Hyperhomocysteinemia as a risk factor for arterial and venous
thrombotic disease. Int J Clin Lab Res 1997; 27:139-44.
14. Girelli D, Friso S, Trabetti E, et al. Methy-leneletrahydrofolate reductase
C677 T mutation, plasma homocysteine, and folate in subjects from Northern Italy
with or without angiographically documented severe coronary atherosclerotic
disease: evidence for an important genetic - environmental interaction. Blood
1998; 91:4158-63.
15. Seligsohn U, Zivelin A. Thrombophilia as a multigenic disorder. Thromb Haemost
1997; 78:297-301.
16. Tαμπακούδης Π. Προεκλαμψία - Παθογένεια και παράγοντες κινδύνου. Eλληνική
Mαιευτική και Γυναικολογία 2001; 13(3):141-59.
17. Seligsohn U, Zivelin A. Thrombophilia as a multigenic disorder. Thromb Haemost
1997; 78:297-301.
18. Tαμπακούδης Π, Kανονίδης I. Θρομβοεμβολικά επεισόδια κατά την κύηση και
τη λοχεία. Eλληνική Mαιευτική και Γυναικολογία 1991; 4(3):180-94.
19. Greer IA. Haemostasis and thrombosis in preg-nancy. In: Bloom AL, Forbes
CD, Thomas DP, Tuddenham EGD, (eds). Haemostasis and Thrombosis. Edinburgh:
Churchill Livingstone, 1994.
20. Clark P, Brennand J, Conkie J, McCall F, Greer I, Walker I. Activated protein
C sensitivity, protein C, protein S, coagulation in normal pregnancy. Thromb
Haemost 1998; 79:1166-70.
21. Heeb MJ, Kojima Y, Greengard JS, Griffin JH. Activated protein C resistance:
molecular mechanisms based on studies using purified Gln 506 factor V. Blood
1995; 85:3405-11.
22. Shen L, He X, Dahlback B. Synergistic cofactor function of factor V and
protein S to activate protein C in the inactivation of the factor VIIIa-factor
IXa complex - species specific interactions of components of the protein C anticoagulant
system. Thromb Haemost 1997; 78:1030-6.
23. Butenas S, vanΥt Veer C, Mann KG. "Normal" thrombin generation.
Blood 1999; 94:2169-78.
24. Smirnov MD, Safa O, Esmon NL, Esmon CT. Inhibition of activated protein
C anticoagulant activity by prothrombin. Blood 1999; 94:3839-46.
25. Zivelin A, Griffin JH, Xu X, et al. A single genetic origin for a common
Caucasian risk factor for venous thrombosis. Blood 1997; 89:397-402.
26. Zivelin A, Rosenberg N, Faier S, et al. A single genetic origin for the
common prothrombotic G20210A polymorphism in the prothrombin gene. Blood 1998;
92:1119-24.
27. Miletich J, Sherman L, Broze G. Absence of thrombosis in subjects with heterozygous
protein C deficiency. N Engl J Med 1987; 317:991-6.
28. Tait RC, Walker ID, Reitsma PH, et al. Prevalence of protein C deficiency
in the healthy population. Thromb Haemost 1995; 73:87-93.
29. Koster T, Rosendaal FR, Briet E, et al. Protein C deficiency in a controlled
series of unselected outpatients: an infrequent but clear risk factor for venous
thrombosis (Leiden Thrombophilia Study). Blood 1995; 85:2756-61.
30. Heijboer H, Brandjes DPM, Buller HR, Sturk A, Ten Cate JW. Deficiencies
of coagulation - inhibiting and fibrinolytic protein in outpatients with deep
- vein thrombosis. N Engl J Med 1990; 323:1512-6.
31. Pabinger I, Brucker S, Kyrle PA, et al. Hereditary deficiency of antitrhombin
III, protein C and protein S: prevalence in patients with a history of venous
thrombosis and criteria for rational patient screening. Blood Coagul Fibrinolysis
1992; 3:547-53.
32. Tabernero MD, Tomas JF, Alberca I, Orfao A, Borrasca AI, Vicente V. Incidence
and clinical characteristics of hereditary disorders associated with venous
thrombosis. Am J Hematol 1991; 36:249-54.
33. Ben-Tal O, Zivelin A, Seligsohn U. The relative frequency of hereditary
thrombotic disorders among 107 patients with thrombophilia in Israel. Thromb
Haemost 1989; 61:50-4.
34. Horellou MH, Conard J, Bertina RM, Samama M. Congenital protein C deficiency
and thrombotic disease in nine French families. BMJ 1984; 289:1285-7.
35. Gladson CL, Scharrer I, Hach V, Beck KH, Griffin JH. The frequency of type
I heterozygous protein S and protein C deficiency in 141 unrelated young patients
with venous thrombosis. Thromb Haemost 1988; 59:18-22.
36. Winkler UH. Blood coagulation and oral con-traceptives. A critical review.
Contraception 1998; 57:203-9.
37. Salomon O, Steinberg DM, Zivelin A, et al. Single and combined prothrombotic
factors in patients with idiopathic venous thromboembolism: prevalence and risk
assessment. Arterioscler Thromb Vasc Biol 1999; 19:511-8.
38. Tait RC, Walker ID, Perry DJ, et al. Prevalence of antitrhombin deficiency
in the healthy population. Br J Haematol 1994; 87:106-12.
39. De Stefano V, Chiusolo P, Paciaroni K, Leone G. Epidemiology of factor V
Leiden: clinical implications. Semin Thromb Hemost 1998; 24:367-79.
40. Ehrenforth S, von Depka Prondsinski M, Aygoren - Pursun E, Nowak-Gottl U,
Shcarrer I, Ganser A. Study of the prothrombin gene 20210 GA variant in FV:
Q506 carriers in relationship to the presence or absence of juvenile venous
thromboembolism. Arterioscler Thromb Vasc Biol 1999; 19:276-80.
41. Hillarp A, Zoller B, Svensson PJ, Dahlback B. The 20210A allele of the prothrombin
gene is a common risk factor among Swedish outpatients with verified deep venous
thrombosis. Thromb Haemost 1997; 78:990-2.
42. Eichinger S, Minar E, Hirschl M, et al. The risk of early recurrent venous
thromboembolism after oral anticoagulant therapy in patients with the G20210A
transition in the prothrombin gene. Thromb Haemost 1999; 8:14-7.
43. Ferraresi P, Marchetti G, Legnani E, et al. The heterozygous 20210 G/A prothrombin
genotype is associated with early venous thrombosis in inherited thrombophilias
and is not increased in frequency in artery disease. Arterioscler Thromb Vasc
Biol 1997; 17:2418-22.
44. Tosetto A, Missiaglia E, Frezzato M, Rodeghiero E. The VITA project: prothrombin
G202010A mutation and venous thromboembolism in the general population. Thromb
Haemost 1999; 82:1395-8.
45. Leroyer C, Mercier B, Oger E, et al. Prevalence of 20210A allele of the
prothrombin gene in venous thromboembolism patients. Thromb Haemost 1998; 80:49-51.
46. Dilley A, Austin H, Hooper WC, et al. The prevalence of the prothrombin
20210G-to-A variant in blacks: infants, patients with venous thrombosis, patients
with myocardial infarction and control subjects. J Lab Clin Med 1998; 132:1-4.
47. Dilley A, Austin H, El-Jamil M, et al. Genetic factors associated with Thrombosis
in pregnancy in a United States population. Am J Obstet Gynecol 2000; 183:1271-7.
48. Souto JC, Coll I. Llobet D, et al. The prothrombin 20210A allele is the
most prevalent genetic risk factor for venous thromboembolism in the Spanish
population. Thromb Haemost 1998; 80:366-9.
49. Alhenc-Gelas M, Arnaud E, Nicaud V, et al. Venous thromboembolic disease
and the prothrombin, methylene tetrahydrofolate reductase and factor V genes.
Thromb Haemost 1999; 81:506-10.
50. Corral J, Gonzales - Conejero R, Lozano ML, Rivera J, Heras I, Vicente V.
The venous thrombosis risk factor 20210A allele of the prothrombin gene is not
a major risk factor for arterial thrombotic disease. Br J Haematol 1997; 99:304-7.
51. Brown K, Luddington R, Williamson D, Baker P, Baglin T. Risk of venous thromboembolism
associated with a G to A transition at position 20210 in the 3Υ- untranslated
region of the prothrombin gene. Br J Haematol 1997; 98:907-9.
52. Hainaut P, Gala JL, Lesage V, et al. The prothrombin gene G20210A variant
in an unselected thromboembolic population: a Belgian prospective clinical study.
Acta Clin Belg 1998; 53:344-8.
53. Howard TE, Marusa M, Boisza J, et al. The prothrombin gene 3Υ - untranslated
region mutation is frequently associated with factor V Leiden in thrombophilic
patients and shows ethnic - specific variation in the allele frequency. Blood
1998; 91:1092.
54. Ridker PM, Hennekens CH, Miletich JP. G20210A mutation in prothrombin gene
and risk of myocardial infarction, stroke, and venous thrombosis in a large
cohort of US men. Circulation 1999; 99:999-1004.
55. Margaglione M, Brancaccio V, Giuliani N, et al. Increased risk for venous
thrombosis in carriers of the prothrombin G > A20210 gene variant. Ann Intern
Med 1998; 129:89-93.
56. Rosendaal FR, Doggen CJM, Zivelin A, et al. Geographic distribution of the
20210 G to A prothrombin variant. Thromb Haemost 1998; 79:706-8.
57. Rees DC, Chapman NH, Webster MT, Guerreiro JF, Rochette J, Clegg JB. Born
to clot: the European burden. Br J Haematol 1999; 105:564-6.
58. De Stefano V, Chiusolo P. Paciaroni K, et al. Prevalence of the factor II
G20210A mutation in symptomatic patients with inherited thrombophilia. Thromb
Haemost 1998; 80:342-3.
59. Koeleman BPC, Reitsma PH, Allaart CF, Bertina RM. Activated protein C resistance
as an additional risk factor for thrombosis in protein C - deficient families.
Blood 1994; 84:1031-5.
60. Zoller B, Berntsdotter A, Garcia de Frutos P, Dahlback B. Resistance to
activated protein C as an additional genetic risk factor in hereditary deficiency
of protein S. Blood 1995; 85:3518-23.
61. Koeleman PBC, van Rumpt D, Hamulyak K, Reitsma PH, Bertina RM. Factor V
Leiden: an additional risk factor for thrombosis in protein S deficient families?
Thromb Haemost 1995; 74:580-3.
62. van Boven HH, Vandenbroucke JP, Briet E, Rosendaal FR. Gene - gene and gene
- environment interactions determine risk of thrombosis in families with inherited
antithrombin deficiency. Blood 1999; 94:2590-4.
63. De Stefano V, Martinelli I, Mannucci PM, et al. The risk of recurrent deep
venous thrombosis among heterozygous carriers of both factor V Leiden and the
G20210A prothrombin mutation. N Engl J Med 1999; 341:801-6.
64. Ridker PM, Hennekens CH, Selhub J, Miletich JP, Malinow MR, Stampfer MJ.
Interrelation of hyperhomocyst(e)inemia, factor V Leiden, and risk of future
venous thromboembolism. Circulation 1997; 95:1777-82.
65. De Stefano V, Zappacosta B, Persichilli S, et al. Prevalence of mild hyperhomocysteinaemia
and association with thrombophilic genotypes (factor V Leiden and prothrombin
G20210A) in Italian patients with venous thromboembolic disease. Br J Heamatol
1999; 106:564-8.
66. Finazzi G, Caccia R, Barbui T. Different prevalence of thromboembolism in
the subtypes of congenital antithrombin III deficiency: review of 404 cases.
Thromb Haemost 1987; 58:1094.
67. Boyer C, Wolf M, Vedrenne J, Meyer D, Larrieu MJ. Homozygous variant of
antithrombin III: AT III Fontainebleu. Thromb Haemost 1986; 56:18-22.
68. Faioni EM, Franchi F, Bucciarelli P, et al. Coinheritance of the HR2 haplotype
in the factor V gene confers an increased risk of venous thromboembolism to
carriers of factor V R 506Q (factor V Leiden). Blood 1999; 94:3062-6.
69. Williamson D, Brown K, Luddington R, Baglin T. Factor V Cambridge: a new
mutation (Arg306 > Thr) associated with resistance to activated protein C.
Blood 1998; 91:1140-4.
70. de Visser MCH, Rosendaal FR, Bertina RM. A reduced sensitivity for activated
protein C in the absence of factor V Leiden increases the risk of venous thrombosis.
Blood 199; 93:1271-6.
71. Ray JG. Meta-analysis of hyperhomocysteinemia as a risk factor for venous
thromboembolic disease. Arch Intern Med 1998; 158:2101-6.
72. Kraaijenhagen RA, Anker PS, Koopman MMW, et al. High plasma concentration
of factor VIIIc is a major risk factor for venous thromboembolism. Thromb Haemost
2000; 83:5-9.
73. van Hulckama Vlieg A, van der Linden IK, Bertina RM, Rosendaal FR. High
levels of factor IX increase the risk of venous thrombosis. Blood 2000; 95:3678-82.
74. Meijers JCM, Tekelenburg WLH, Bouma BN, Bertina RM, Rosendaal FR. High levels
of coagulation factor XI as a risk factor for venous thrombosis. N Engl J Med
2000; 342:696-701.
75. Koster T, Rosendaal FR, Reitsma PH, van der Velden PA, Briet E, Vandenbroucke
JP. Factor VII and fibrinogen levels as risk factors for venous thrombosis:
a case - control study of plasma levels and DNA polymorphisms - the Leiden Thrombo-philia
Study (LETS). Thromb Haemost 1994; 71:719-22.
76. Emmerich J, Alhence - Gelas M, Aillaud MF, et al. Clinical features in 36
patients homozygous for the ARG 506 > GLN factor V mutation. Thromb Haemost
1997; 77:620-3.
77. Martineli I, Mannucci PM, De Stefano V, et al. Different risks of thrombosis
in four coagulation defects associated with inherited thrombophilia: a study
of 150 families. Blood 1998; 92:2353-8.
78. Middeldorp S, Henkens CM, Koopman MM, et al. The incidence of venous thromboembolism
in family members of patients with factor V Leiden mutation and venous thrombosis.
Ann Intern Med 1998; 128:15-20.
79. Bucciarelli P, Rosendaal FR, Thipodi A, et al. Risk of venous thromboembolism
and clinical mani-festations in carriers of antithrombin, protein C, protein
S deficiency, or activated protein C resistance: a multicenter collaborative
family study. Arterioscler Thromb Vasc Biol 1999; 19:1026-33.
80. Simioni P, Sanson PJ, Prandoni P, et al. Incidence of venous thromboembolism
in families with inherited thrombophilia. Thromb Haemost 1999; 81:198-202.
81. Sanson BJ, Simioni P, Tormene D, et al. The incidence of venous thromboembolism
in asympto-matic carriers of a deficiency of antithrombin, protein C, protein
S: a prospective cohort study. Blood 1999; 94:3702-6.
82. Girling J, de Swiet M. Inherited thrombophilia and pregnancy. Curr Opin
Obstet Gynecol 1998; 10:135-44.
83. Friederich PW, Sanson BJ, Simioni P, et al. Frequency of pregnancyrelated
venous thrombo-embolism in anticoagulant factor - deficient women: Ann Intern
Med 1997; 126:835, 127:1138.
84. Grandone E, Margaglione M, Colaizzo D, et al. Genetic susceptibility to
pregnancy - related venous thromboembolism: roles of factor V Leiden, prothrombin
G20210A, and methylenetetrahydro-folate reductase C677T mutations. Am J Obstet
Gynecol 1998; 179:1324-8.
85. Gerhardt A, Scharf RE, Beckmann MW, et al. Prothrombin and factor V mutations
in women with a history of thrombosis during pregnancy and the pueperium. N
Engl M Jed 2000; 342:374-80.
86. Preston FE, Rosendaal FR, Walker ID, et al. Increased fetal loss in women
with heritable thrombophilia. Lancet 1996; 348:913-6.
87. Martinelli I, Taioli E, Cetin I, et al. Mutations in coagulation factors
in women with unexplained late fetal loss. N Engl J Med 2000; 343:1015-8.
88. Sanson BJ, Friederich PW, Simioni P, et al. The risk of abortion and stillbirth
in antitrhombin-, protein C, and protein S - deficient women. Thromb Haemost
1996; 75:387-8.
89. Ridker PM, Miletich JP, Buring JE, et al. Factor V Leiden mutation as a
risk factor for recurrent pregnancy loss. Ann Intern Med 1998; 128:1000-3.
90. Kupferminc MJ, Eldor A, Steinman N, et al. Increased frequency of genetic
thrombophilia in women with complications of pregnancy. N Engl J Med 1999; 340:9-13.
91. Kyrle PA, Minar E, Furschi M, et al. High plasma levels of factor VIII and
the risk of recurrent venous thromboembolism. N Engl J Med 2000; 343:457-62.
92. den Heijer M, Blom HJ, Gerrits WBJ, et al. Is hyperhomocysteinemia a risk
factor for recurrent venous thrombosis? Lancet 1995; 345:882-5.
93. Schulman S, Svenungsson E, Granqvist S. Anti-cardiolipin antibodies predict
early recurrence of thromboembolism and death among patients with venous thromboembolism
following anticoagulant therapy. Am J Med 1998; 104:332-8.
94. Fisher M, Fernandez JA, Ameriso SF, et al. Activated protein C resistance
in ischemic stroke not due to factor V arginine 506 > glutamine mutation.
Stroke 1996; 27:1163-6.
95. Zivelin A, Gitel S, Griffin JH, et al. Extensive venous and arterial thrombosis
associated with an inhibitor to activated protein C. Blood 1999; 94:895-901.
96. Schulman S. Duration of anticoagulants in acute or recurrent venous thromboembolism.
Curr Opin Pulm Med 2000; 6:321-5.
97. McColl MD, Tait RC, Walker ID, Perry DJ, McCall F, Conkie JA. Low thrombosis
rate seen in blood donors and their relatives with inherited defi-ciencies of
antithrombin and protein C: corre-lation with type of defect, family history,
and absence of the factor V Leiden mutation. Blood Coag Fibrinol 1996; 7:689-94.
98. Walker ID. Inherited bleeding and thrombotic disorders. In: Bannar J. (ed.)
Recent Advances in Obstetrics and Gynaecology. Churchill Livingstone, 1998.
99. Hunt B, Doughty H, Majundar G, et al. Thromboprophylaxis with low molecular
weight heparin (Fragmin) in high risk pregnancies. Thromb Haemost 1997; 77:39-43.
100. Nelson - Piercy C, Letsky E, de Swiet M. Low - molecular - weight heparin
for obstetric thromboprophylaxis: experience of sixty - nine pregnancies in
sixty - one women at high risk. Am J Obstet Gynecol 1997; 176:1062-8.
101. Melissari E, Parker CJ, Wilson NV, et al. Use of low molecular weight heparin
in pregnancy. Thromb Haemost 1992; 68:652-6.
102. Alving B, Spivak J. Deloughery T. Consultative hematology: hemostasis and
transfusion issues in surgery and critical care medicine - strategies to avoid
spinal/epidural hematomas in perioperative patients receiving LMW heparin. American
Society for Hematology Education Program Book, 1998:320-41.
Aλληλογραφία:
Π. Tαμπακούδης
Πλ. Συντριβανίου 4
54621 Θεσσαλονίκη
Tηλ: 0310228497