ΑΡΘΡΟ ΕΝΗΜΕΡΩΣΗΣ
Η χρήση εμβολίων στην
πρόληψη και
τη θεραπεία του καρκίνου του
τραχήλου της μήτρας
B.Π. Πετροπούλου
Π.Β. Πετρόπουλος
Αλληλογραφία:
Βασιλική Π. Πετροπούλου
MR Pharms, MSc, PhD
Άλσους 13, Ωραιόκαστρο, 57013
Τηλ. 2310697567
Fax: 2310698909
E-mail: pjv@med.auth.gr
Kατατέθηκε 18/11/2004
Eγκρίθηκε 15/12/2004
Περίληψη
Η στενή σχέση ανάμεσα στην υψηλού κινδύνου λοίμωξη από τον ιό των θηλωμάτων
(HPV) και τον καρκίνο του τραχήλου έχει αποδειχθεί με την ανίχνευση του HPV
DNA σχεδόν σε όλους τους κακοήθεις όγκους του τραχήλου της μήτρας. Η σχέση αυτή
οδηγεί στο συμπέρασμα ότι ο καρκίνος του τραχήλου μπορεί να προληφθεί ή να θεραπευθεί
με εμβόλια έναντι του HPV. H L1, κύρια πρωτεΐνη του ιικού καψιδίου, έχει την
ενδογενή ικανότητα να σχηματίζει μόρια που προσομοιάζουν προς τον ιό (virus
like particles - VLPs). Από διάφορες μελέτες φαίνεται ότι τα εμβόλια που περιέχουν
HPV L1 VLPs υπόσχονται ικανοποιητική προφύλαξη, ενώ αυτά που περιέχουν L2 VLPs
πρέπει να μελετηθούν περαιτέρω σε ασθενείς. Διάφορα θεραπευτικά εμβόλια που
στοχεύουν τα ογκογονίδια Ε6 και Ε7 εμφανίζουν τις καλύτερες προοπτικές για τον
έλεγχο της κακοήθειας που έχει σχέση με τον HPV. Σήμερα δοκιμάζονται οι ογκοπρωτεΐνες
Ε6 και Ε7 σε vectors (πεπτίδια και πρωτεΐνες), σε νουκλεϊνικά οξέα, ή σε κυτταροεξαρτώμενα
εμβόλια.
Η παρασκευή ενός αποτελεσματικού προφυλακτικού εμβολίου θα εδραιώσει την ανάγκη
προγραμμάτων προσυμπτωματικού ελέγχου του πληθυσμού, ενώ ο θεραπευτικός εμβολιασμός
θα μπορέσει να συνεισφέρει θετικά στη συμβατική θεραπεία των καλοήθων και των
κακοήθων όγκων ή ακόμα και να την αντικαταστήσει. Παρά το γεγονός ότι οι δυσχέρειες
στον σχεδιασμό των ανοσοθεραπειών είναι πολλές, υπάρχει αισιοδοξία και αναμένεται
ότι στις επόμενες δεκαετίες θα σημειωθούν σημαντικές αλλαγές στον τρόπο αντιμετώπισης
του καρκίνου του τραχήλου και των προκαρκινικών καταστάσεων. Ένα εμβόλιο κατά
του ιού των θηλωμάτων, το οποίο θα συμβάλλει τόσο στην πρόληψη της HPV λοίμωξης,
όσο και στην αντιμετώπιση της ήδη εγκατεστημένης νόσου, θα επηρεάσει σημαντικά
την καταπολέμηση του καρκίνου του τραχήλου της μήτρας που προσβάλλει εκατομμύρια
γυναίκες σε όλο τον κόσμο.
Όροι ευρετηρίου: HPV λοίμωξη, καρκίνος του τραχήλου, προφυλακτικά εμβόλια, θεραπευτικά εμβόλια.
ΕΙΣΑΓΩΓΗ
Ο καρκίνος του τραχήλου της μήτρας θεωρείται διεθνώς η δεύτερη αιτία θανάτου.
Παρά το γεγονός ότι η εφαρμογή των προληπτικών κυτταρολογικών εξετάσεων ελάττωσε
την εμφάνιση της νόσου στις Δυτικές χώρες, τα ποσοστά παραμένουν αρκετά υψηλά.
Η ανίχνευση του DNA του ιού των θηλωμάτων (human papilloma virus - HPV) σχεδόν
σε όλους τους όγκους οδήγησε στο συμπέρασμα ότι υπάρχει στενή σχέση ανάμεσα
στην HPV λοίμωξη και στον καρκίνο του τραχήλου,(1) καθώς επίσης και στο εξίσου
σημαντικό συμπέρασμα ότι ο καρκίνος του τραχήλου μπορεί να προληφθεί ή να θεραπευτεί
με εμβόλια έναντι του HPV. Στο άρθρο αυτό επιχειρείται μια ανασκόπηση της πορείας
της HPV λοίμωξης, εξετάζεται ο ρόλος της φυσικής ανοσίας στην πορεία της λοίμωξης
και αναλύεται ο σχεδιασμός της παρασκευής προληπτικών και θεραπευτικών εμβολίων
έναντι του καρκίνου του τραχήλου της μήτρας.
ΕΞΕΛΙΞΗ
ΤΗΣ HPV ΛΟΙΜΩΞΗΣ
Ο ιός των θηλωμάτων (HPV) είναι ένας μικρός ιός της οικογένειας Papovαviridae,
με δίκλωνο DNA.(2) Το γένωμα του HPV έχει μέγεθος 7,9kb και περιλαμβάνει 8 ανοικτά
πλαίσια ανάγνωσης (open reeding frames - ORFs), που κωδικοποιούν 6 πρώιμες (early
- E) τις E1, E2, E4, E5, E6, E7, και 2 όψιμες (late - L) τις L1 και L2 πρωτεΐνες.(3)
Ο διαχωρισμός σε πρώιμα και όψιμα ιικά γονίδια γίνεται με βάση τον χρόνο εμφάνισής
τους κατά τη φυσική εξέλιξη της HPV λοίμωξης. Μια μεγάλη ρυθμιστική περιοχή
(long control region - LCR) περιέχει προαγωγικές και ενισχυτικές ακολουθίες
και τα γονίδια αντιγραφής του ιού.(4,5) Ο HPV προσβάλλει αποκλειστικά επιθηλιακά
κύτταρα και για την ολοκλήρωση του κύκλου της ζωής του εξαρτάται απόλυτα από
τη διαδικασία κερατινοποίησης του επιθηλίου.(6) Τα κύτταρα της βασικής στιβάδας
του επιθηλίου του τραχήλου της μήτρας μεταναστεύουν προοδευτικά προς υπερκείμενα
στρώματα, και αντικαθίστανται διαρκώς με νεότερα κύτταρα που προέρχονται από
τη βασική στιβάδα. Η επιφανειακή στιβάδα του επιθηλίου περιλαμβάνει κύτταρα
απύρηνα, πλήρως κερατινοποιημένα, τα οποία τελικά αποφολιδώνονται. Τα σωματίδια
του ιού συνδέονται και μολύνουν τα κύτταρα της βασικής στιβάδας του επιθηλίου
στη ζώνη μετάπτωσης του τραχήλου. Αυτό μπορεί να έχει σχέση με κάποια τοπική
βλάβη ή μικροτραυματισμούς που διαταράσσουν την ακεραιότητα του επιθηλίου και
επιτρέπουν τη διείσδυση του ιού. Οι πρωτεΐνες L1 και L2 του καψιδίου του ιού
πιστεύεται ότι διαμορφώνουν συγκεκριμένη δομή, η οποία είναι ικανή να αντιδρά
με υποδοχείς της επιφάνειας του κυττάρου, διευκολύνοντας την είσοδο του DNA
του ιού μέσα στο κύτταρο.(7-9)
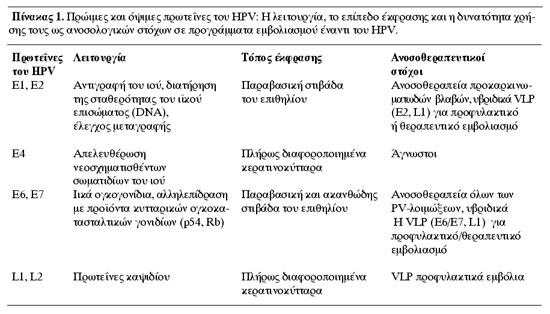
Η έκφραση των γονιδίων του ιού σχετίζεται με τη διαδικασία ωρίμανσης και αποφολίδωσης
των κυττάρων του επιθηλίου (πίνακας 1). Οι πρωτεΐνες Ε1 και Ε2 εκφράζονται στα
κύτταρα της παραβασικής στιβάδας, όπου είναι απαραίτητες για τη διατήρηση της
σταθερότητας του ιϊκού επισώματος (αυτόνομο, αυτο-αντιγραφόμενο εξω-χρωμοσωμικό
ιικό DNA)(10) και την έναρξη της αναπαραγωγής του ιού.(11,12) Η Ε2 λειτουργεί
ως ρυθμιστής της παραγωγής των πρωτεϊνών Ε6 και Ε7 του ιού.(13) Οι πρωτεΐνες
αυτές παρεμβαίνουν στους ρυθμιστικούς μηχανισμούς του κυττάρου-ξενιστή και επαναδραστηριοποιούν
τη σύνθεση του DNA και των κυτταρικών πρωτεϊνών, με σκοπό να διευκολύνουν την
αντιγραφή του DNA του ιού.(14) Οι πρωτεΐνες L1 και L2 εκφράζονται μόνο στα τελικά
διαφοροποιημένα κερατινοκύτταρα των ανώτερων στρωμάτων του επιθηλίου,(15,16)
όπου επίσης εκφράζεται και η πρωτεΐνη Ε4. Η Ε4 πιστεύεται ότι διευκολύνει την
απελευθέρωση των νεοσχηματιζόμενων σωματιδίων του ιού από το κύτταρο-ξενιστή.(17)
Ο κύκλος ζωής του ιού ολοκληρώνεται με την παραγωγή και τη συνάθροιση των νέων
ιϊκών σωματιδίων, την απελευθέρωσή τους από το ώριμο κερατινοκύτταρο και την
επακόλουθη προσβολή νέων κυττάρων-ξενιστών.
Οι πρωτεΐνες Ε6 και Ε7 του ογκογόνου HPV συνδέονται με τα παράγωγα των κυτταρικών
ογκοκατασταλτικών γονιδίων p53 και ρετινοβλαστώματος (Rb) αντίστοιχα. Η σύνδεση
της υψηλού κινδύνου Ε6 με το p53 διευκολύνει την εξάπλωση και τη λειτουργική
έκπτωση του p53,(18) με αποτέλεσμα την απώλεια της εξαρτώμενης από το p53 απόπτωσης
του επιθηλίου και την αναστολή του κυτταρικού κύκλου στη φάση G1.(19) Η ένωση
της υψηλού κινδύνου Ε7 με το Rb οδηγεί στη διαταραχή του φυσιολογικού μηχανισμού
ελέγχου του κυτταρικού κύκλου, με συνέπεια τον ανεξέλεγκτο κυτταρικό πολλαπλασιασμό.(20)
Σε καλοήθεις αλλοιώσεις το γένωμα του ιού διατηρείται σταθερά, ως εξω-χρωμοσωμικό
επίσωμα, στο κυτταρόπλασμα του κυττάρου ξενιστή. Η κακοήθης εξαλλαγή των κυττάρων
έχει ως αποτέλεσμα την ενσωμάτωση του ιϊκού DNA στο γένωμα του ξενιστή,(21)
τη διάσπαση του γονιδίου που κωδικοποιεί την πρωτεΐνη Ε2 και επομένως την απώλεια
έκφρασης της συγκεκριμένης πρωτεΐνης.(22,23) Επειδή η Ε2 είναι απαραίτητη για
την καταστολή των Ε6 και Ε7 ογκοπρωτεϊνών, η απώλειά της προκαλεί την υπερέκφραση
αυτών των ογκογονιδίων.(24) Η συνδυασμένη δράση των Ε6 και Ε7 ογκογονιδίων δημιουργεί
το κατάλληλο περιβάλλον που οδηγεί στον πολλαπλασιασμό των κυττάρων, ενώ παράλληλα
διαταράσσονται οι φυσιολογικοί μηχανισμοί ελέγχου του κυτταρικού κύκλου. Αυτό
επιτρέπει να εμφανίζονται περιοδικές μιτώσεις και ανεξέλεγκτα λάθη, τα οποία
συμβάλλουν στην εξαλλαγή των κυττάρων.(25) Είναι πλέον βέβαιο ότι τα ογκογονίδια
Ε6 και Ε7 είναι ισχυροί καρκινογόνοι παράγοντες, οι οποίοι μπορεί να προκαλέσουν
αέναη κυτταρική διαίρεση και, σε συνδυασμό με άλλους παράγοντες, καρκινογένεση.(26)
Η ανάπτυξη του καρκίνου του τραχήλου είναι τελικά μια σταδιακή συνδυασμένη διεργασία
επίμονης HPV λοίμωξης,(27) διαταραχής των ιϊκών ογκογονιδίων(28) και συσσώρευσης
περαιτέρω γενετικών δεδομένων(25) που οδηγούν στη νεοπλασία.

ΦΥΣΙΚΗ ΑΝΟΣΙΑ
ΚΑΙ ΕΛΕΓΧΟΣ ΤΗΣ HPV ΛΟΙΜΩΞΗΣ
Οι HPV λοιμώξεις του κατώτερου γεννητικού σωλήνα είναι εξαιρετικά συχνές στις
νεαρές σεξουαλικά ενεργείς γυναίκες. Οι περισσότερες λοιμώξεις αντιμετωπίζονται
έγκαιρα από το αμυντικό ανοσολογικό σύστημα, χωρίς να δημιουργούν κλινικά επακόλουθα.(29,30)
Οι επίμονες λοιμώξεις από ογκογόνους ιούς των θηλωμάτων σχετίζονται με την προκαρκινωματώδη
τραχηλική ενδοεπιθηλιακή νεοπλασία (cervical intraepithelial neoplasia - CIN)
και το διηθητικό καρκίνο του τραχήλου.(28,31,32) Περίπου 25 από τους 80 και
πλέον τύπους του HPV προκαλούν φλεγμονή του γεννητικού συστήματος. Υπολογίζεται
ότι το 50% των περιπτώσεων καρκίνου του τραχήλου έχει σχέση με την HPV16 λοίμωξη.(33)
Οι γυναίκες με ανοσοκαταστολή λόγω HIV λοίμωξης ή οι ασθενείς υπό μακρά ανοσοκατασταλτική
θεραπεία λόγω μεταμόσχευσης έχουν αυξημένη πιθανότητα ανάπτυξης κονδυλωμάτων,
CIN και καρκίνου του τραχήλου, καταστάσεις που έχουν άμεση σχέση με την HPV
λοίμωξη.(34-38) Αυτή η παρατήρηση οδήγησε στην υπόθεση ότι οι ανοσολογικοί παράγοντες
ενέχουν σημαντικό ρόλο στη φυσική αντιμετώπιση των HPV λοιμώξεων. Περαιτέρω
ενδείξεις επιβεβαίωσης της παραπάνω θεωρίας προκύπτουν από τη μελέτη των καλοήθων
κονδυλωμάτων, στα οποία παρατηρούνται μεγάλες διηθήσεις κυρίως Τ-λεμφοκυττάρων,
τα οποία σχετίζονται άμεσα με την υποχώρηση της νόσου,(39-41) χωρίς ωστόσο να
έχουν ακόμη εξακριβωθεί οι ακριβείς μηχανισμοί. Προκειμένου να υπάρξουν οι κατάλληλες
προϋποθέσεις για τη δημιουργία ενός αποτελεσματικού εμβολίου, πρέπει να γίνουν
κατανοητοί οι ανοσολογικοί παράγοντες - κλειδιά που σχετίζονται με τη δράση
του ιού.
Τα αντισώματα έναντι των πρωτεϊνών του καψιδίου του ιού φαίνεται να έχουν σχέση
με την έκθεση στον HPV.(42) Ειδικά τα αντί-L1 αντισώματα ανιχνεύονται σε γυναίκες
με επίμονη HPV λοίμωξη και high grade CIN, σπανιότερα όμως σε ασθενείς με διηθητικό
καρκίνο του τραχήλου, στον οποίο ο ιός ενσωματώνεται και αναστέλλεται η εξάπλωση
της λοίμωξης.(43) Τα αδρανοποιητικά αντισώματα πιθανώς να παίζουν σημαντικό
ρόλο στην καταπολέμηση της λοίμωξης, επειδή όμως ο HPV είναι ενδοκυττάριος ιός,
κατά τη διάρκεια του κύκλου της ζωής του προστατεύεται από τη δράση των αντισωμάτων
του ξενιστή. Συνεπώς, είναι μικρές οι πιθανότητες αντιμετώπισης της λοίμωξης
από τα συγκεκριμένα αντισώματα.(44) Τα φυσιολογικά Τ-λεμφοκύτταρα, τα οποία
συσσωρεύονται ως απάντηση στις πρωτεΐνες του HPV, έχουν ανιχνευτεί σε γυναίκες
με HPV λοίμωξη, αλλά δεν έχει διευκρινιστεί κατά πόσο το γεγονός αυτό είναι
συνέπεια της λοίμωξης από τον ιό ή αμυντικός μηχανισμός καταπολέμησης της λοίμωξης.
Ειδικά αντι-HPV κυτταροτοξικά Τ-λεμφοκύτταρα (cytotoxic T lymphocytes - CLT)
έναντι των πρωτεϊνών Ε6 και Ε7 του HPV έχουν βρεθεί σε γυναίκες με CIN3 και
καρκίνο του τραχήλου της μήτρας.(45) Τα ειδικά αυτά κυτταροτοξικά Τ-λεμφοκύτταρα
(CTL) βρίσκονται σε μεγαλύτερες συγκεντρώσεις στις περιοχές έκθεσης των αντιγόνων
του ιού, στους όγκους και στους επιχώριους λεμφαδένες.(46) Ο ακριβής καθορισμός
του ρόλου των CLT (CD8) στην πρόληψη, τον έλεγχο ή την εκρίζωση της νόσου αποτελεί
συνεχή πρόκληση. Αρκετές μελέτες έχουν καταλήξει στο συμπέρασμα ότι υπάρχει
σχέση μεταξύ της δράσης των ειδικών αντι- HPV Τ-βοηθητικών λεμφοκυττάρων και
της εκρίζωσης του ιού,(47,48) ωστόσο ο ακριβής ρόλος αυτής της δράσης στην εξέλιξη
της λοίμωξης είναι ένα ενδιαφέρον ερευνητικό πεδίο.
Αναλυτικότερα τα Τ- λεμφοκύτταρα, τα οποία συμμετέχουν στην ενεργοποίηση της
χυμικής ανοσίας (διέγερση των Β-κυττάρων), είναι τα Τ4 βοηθητικά (CD4) και τα
Τ3 κατασταλτικά λεμφοκύτταρα (CD3) σε αναλογία 1/3. Απόκλιση αυτής της σχέσης
εμφανίζουν τα άτομα με ασυνήθιστη ευαισθησία στις ιογενείς λοιμώξεις. Η κυτταρολυτική
ικανότητα των CD4, των Β-κυττάρων και των μακροφάγων στον τράχηλο της μήτρας
είναι ανεξάρτητη από τις στεροειδείς ορμόνες. Τα CD4 κύτταρα ενεργοποιούνται
όταν "αντικρίσουν" το αντιγόνο (HPV), το οποίο εμφανίζεται συνδεδεμένο
με τα μόρια μείζονος ιστοσυμβατότητας (major histocomba-tibility comblex - MHC)
κλάσης Ι ή II από τα αντιγονο-παρουσιαστικά κύτταρα (antigen presenting cells
- APCs). Ακολουθεί η ενεργοποίηση των CD3 κυττάρων και η τοπική ενεργοποίηση
των Β-κυττάρων για την παραγωγή των ειδικών αντισωμάτων έναντι του ιού, τα οποία
είναι κυρίως S-IgA.
Οι τοπικές αντισωματικές αντιδράσεις από τα Β-κύτταρα είναι ισχυρότερες, όταν
οι ασθενείς βρίσκονται στη φάση κάθαρσης από τον ιό με τη μεσολάβηση των κυτοκινών.
Η διέγερση των CD4 έχει ως επακόλουθο την παραγωγή διαφόρων κυτοκινών, οι οποίες
με τη σειρά τους συμβάλλουν στην ενεργοποίηση των Τ-κυτταροτοξικών κυττάρων
(CD8), που είναι τα βασικά κύτταρα της ανοσο-επιτήρησης έναντι του ιού και της
ενεργοποίησης των μακροφάγων στην περιοχή της φλεγμονής. Η αναλογία των CD4/CD8
στον τράχηλο είναι 1/2, με σαφή επικράτηση των CD8 κυτταροτοξικών. Τα ιικά πεπτίδια
που βρίσκονται στην επιφάνεια των μολυσμένων κυττάρων προσλαμβάνονται από τα
APCs, κατακερματίζονται, συνδέονται με μόρια MHC κλάσης I και προβάλλονται εκ
νέου στην επιφάνεια των APCs. Τα ενεργοποιημένα, από την IL-2 ή και την INF-γ,
CD8 κυτταροτοξικά αναγνωρίζουν το σύμπλεγμα ιικό αντιγόνο-MHC-I και προσκολλώνται
στην επιφάνεια του μολυσμένου κυττάρου. Ο κυτταρικός θάνατος επιτυγχάνεται είτε
με κυτταροτοξικές ουσίες που περιέχονται στα κοκκία των CD8, με κυριότερη την
περφορίνη, είτε με την επαγωγή της έκφρασης των γονιδίων απόπτωσης των μολυσμένων
κυττάρων, την οποία προάγουν τα CD8-κύτταρα. Τέλος, πρέπει να σημειωθεί ότι
η δράση των CD8-κυττάρων επηρεάζεται από τα επίπεδα των στεροειδών ορμονών.(49)
Η έκταση και ο τύπος της Τ- βοηθητικής (CD4) κυτταρικής ενεργοποίησης στο τραχηλικό
μικροπεριβάλλον και της Τ-ανοσιακής διαμεσολάβησης προς τα Β-κύτταρα και τα
Τ- κυτταροτοξικά εξαρτάται από την έκφραση των MHC, από τα συγκολλητικά μόρια
της κυτταρικής επιφάνειας (CD11a/18, CD50, CD54, CD58 και CD86) και από τις
τοπικές κυτοκίνες, οι οποίες προέρχονται από τα εντός της βλάβης κερατινοκύτταρα
και τα κύτταρα Langerhans. Είναι γνωστό ότι μεταξύ των APCs, τα κύτταρα Langerhans
θεωρούνται τα ικανότερα για να πυροδοτήσουν Τ- κυτταρικές αντιδράσεις. Η απουσία
των APCs οδηγεί στην έναρξη μη επαρκούς ή πλήρως ανεπαρκούς ανοσολογικής αντίδρασης
και είναι απόλυτα τεκμηριωμένη η ελάττωση των APCs στην τραχηλική ενδοεπιθηλιακή
νεοπλασία.
Φαίνεται επίσης σαφώς ότι σημαντικό ρόλο στην ανάπτυξη αντιιικής προστασίας
παίζει ο τύπος των HLA αντιγόνων (MHC), ο οποίος μπορεί να επηρεάσει ως ένα
βαθμό την ικανότητα της ανοσολογικής απόκρισης στην HPV λοίμωξη. Έχει διαπιστωθεί
ότι τα κύτταρα των τραχηλικών όγκων με ενσωματωμένο υψηλού κινδύνου στέλεχος
HPV, υπό την επίδραση στεροειδών ορμονών αναστέλλουν την έκφρασή τους για τα
HLA κλάσης I μόρια και συνεπώς έχουν μειωμένη ικανότητα να παρουσιάζουν HPV-αντιγόνα
στα κυτταροτοξικά Τ-κύτταρα (CD8). Το γεγονός αυτό εξηγεί, γιατί αντενδείκνυται
η χορήγηση αντισυλληπτικών δισκίων ή και άλλων στεροειδών ορμονών σε οποιαδήποτε
μορφή στις γυναίκες με HPV λοίμωξη.(50,51)
Η στενή σχέση ανάμεσα στην επίμονη HPV λοίμωξη και στον καρκίνο του τραχήλου
της μήτρας οδηγεί στο συμπέρασμα ότι ο καρκίνος του τραχήλου είναι δυνατό να
προληφθεί ή να θεραπευτεί με τη χρήση εμβολίων. Στόχος του εμβολιασμού είναι
η πρόκληση ειδικής ανοσίας μακράς διάρκειας έναντι του HPV, ώστε να εμποδιστεί
η μόλυνση ή να υποχωρήσει η ήδη εγκατεστημένη νόσος. Παρά το γεγονός ότι δεν
έχουν βρεθεί ακόμη οι ακριβείς ανοσολογικοί μηχανισμοί που είναι απαραίτητοι
για την καταπολέμηση του HPV, έχουν αρχίσει οι διαδικασίες παρασκευής προφυλακτικών
και θεραπευτικών εμβολίων. Τα προφυλακτικά εμβόλια έχουν ως στόχο να εμποδίσουν
την εγκατάσταση μιας μακρόχρονης λοίμωξης και την επαναλοίμωξη. Τα θεραπευτικά
εμβόλια στοχεύουν στον περιορισμό της ήδη εγκατεστημένης λοίμωξης, τόσο στους
κακοήθεις όσο και στους καλοήθεις όγκους.
ΠΡΟΦΥΛΑΚΤΙΚΑ
ΕΜΒΟΛΙΑ
Οι προφυλακτικοί εμβολιασμοί έχουν ως στόχο την παραγωγή και τη δράση υψηλών
τίτλων αδρανοποιητικών αντισωμάτων έναντι των τύπων του HPV που ανιχνεύονται
στο γυναικείο γεννητικό σύστημα.(52) Η σύνδεση των αντισωμάτων με τα καψίδια
του ιού εμποδίζει την αλληλεπίδραση μεταξύ των σωματιδίων του ιού και των κυτταρικών
υποδοχέων του τραχηλικού επιθηλίου, διευκολύνοντας έτσι τη δράση των οψωνινών
(ανοσοσφαιρίνες και πρωτεΐνη C3b του συμπληρώματος), οι οποίες επάγουν τη φαγοκύτωση
των σωματιδίων του ιού από τα μακροφάγα.(53)
Η παρατήρηση ότι η L1, κύρια πρωτεΐνη του ιικού καψιδίου, έχει την ενδογενή
ικανότητα να σχηματίζει μόρια που προσομοιάζουν προς τον ιό (virus like particles
- VLP) απουσία άλλων γονιδιακών προϊόντων του ιού, προσέφερε ένα μεγάλο τεχνολογικό
πλεονέκτημα.(54) Τα VLP είναι μόρια μορφολογικά όμοια με τα πλήρη σωματίδια
του ιού, με τη διαφορά ότι δεν διαθέτουν το γενετικό υλικό του ιού. Υψηλοί τίτλοι
των ειδικών αδρανοποιητικών αντισωμάτων έναντι του ιού των θηλωμάτων έχουν παρατηρηθεί
σε ζώα, τα οποία είχαν ανοσοποιηθεί με υψηλές δόσεις HPV VLP.(55-57) Ενθαρρυντικά
μηνύματα έχουν προκύψει από πρώιμες μελέτες σε εθελόντριες, στις οποίες διαπιστώθηκε
υψηλό ποσοστό ανοσοποιητικής ικανότητας με τη χρήση των εμβολίων που περιέχουν
HPV VLP.(58) Το Εθνικό Ινστιτούτο Καρκίνου των ΗΠΑ δοκιμάζει την αποτελεσματικότητα
ενός HPV 16 VLP εμβολίου σε 6.000 τυχαία επιλεγμένες γυναίκες στην Κόστα Ρίκα,
σε σχέση με ομάδα ελέγχου. Σκοπός του πειράματος είναι να διευκρινιστεί αν και
κατά πόσο η ανοσοποίηση με τα μόρια VLP μπορεί να προκαλέσει την παραγωγή υψηλών
τίτλων μακρόβιων αντισωμάτων στη γυναικεία γεννητική οδό, ώστε να αποφευχθεί
η μετάδοση του HPV μέσω της σεξουαλικής επαφής.
Πρόσφατα, ο εμβολιασμός μεγάλου αριθμού γυναικών με HPV 16 VLPs έδειξε ότι ο
τύπος αυτός του εμβολίου είναι πολύ αποτελεσματικός στην πρόληψη της ανάπτυξης
ανθεκτικών λοιμώξεων, όπως αποδεικνύεται σε εξετάσεις με PCR.(59) Αποτελέσματα
ερευνών για τον τύπο 16, που περιέχεται στο τετραδύναμο HPV L1 VLP εμβόλιο (τύποι
6, 11, 16, και 18 του HPV) της Merck/APM SD και τους τύπους 16 και 18 που περιέχονται
στο διδύναμο HPV L1 VLP εμβόλιο (τύποι 16 και 18 του HPV), επιβεβαιώνουν την
ικανότητα των L1 VLP εμβολίων για την πρόληψη της HPV λοίμωξης και της δυσπλασίας
του τραχήλου. Το εμβόλιο της Merck/APM SD που περιέχει τον HPV 16 επέδειξε 100%
αποτελεσματικότητα στην πρόληψη της λοίμωξης και της σχετικής με τον HPV 16
CIN σε γυναίκες που δεν λάμβαναν μέτρα πρόληψης. Συνεχιζόμενες μελέτες σε περισσότερα
από 25000 άτομα σε 33 χώρες θα εκτιμήσουν την ασφάλεια και την αποτελεσματικότητα
του εμβολίου της Merck/APM SD τόσο στην πρόληψη της CIN IΙ και ΙΙΙ που συνδέονται
με τον HPV16 και 18, όσο και στην πρόληψη των κονδυλωμάτων που συνδέονται με
τους HPV6 και HPV11. Aν επιβεβαιωθεί η αποτελεσματικότητα του, το τετραδύναμο
εμβόλιο θα είναι διαθέσιμο εντός τριών ετών.(60)
Είναι πιθανό τα εμβόλια VLP να χρησιμοποιηθούν τόσο για την πρόληψη της HPV
λοίμωξης, όσο και για τη θεραπεία της λοίμωξης σε πρώιμο στάδιο, ώστε να αποτραπεί
η επανεμφάνιση της νόσου λόγω επαναδραστηριοποίησης του ιού ή λόγω επαναλοίμωξης.
Στο Μάντσεστερ της Μεγάλης Βρετανίας έχει ξεκινήσει πειραματική μελέτη με τη
χορήγηση εμβολίου που περιέχει HPV 16 L1 VLP. Ο πρωταρχικός στόχος αυτής της
ελεγχόμενης διπλής τυφλής τυχαιοποιημένης μελέτης είναι η συσχέτιση των μέσης
τάξης δυσκαρυωτικών επιχρισμάτων των γυναικών με την ασφάλεια και την ανοσοποιητική
ικανότητα του εμβολίου. Δεύτερος στόχος είναι η αξιολόγηση των κυτταρολογικών
και κολποσκοπικών μεταβολών που ακολουθούν την ανοσοποίηση. Από διάφορες μελέτες
αναδεικνύεται ότι τα εμβόλια που περιέχουν HPV L1 VLPs υπόσχονται ικανοποιητική
προφύλαξη, ενώ αυτά που περιέχουν L2 VLPs πρέπει να εξετασθούν περαιτέρω σε
ασθενείς.(61)
Η συστηματική εφαρμογή ενός αποτελεσματικού προληπτικού εμβολίου έναντι του
HPV αναμένεται μετά από αρκετά χρόνια και αφού ξεπεραστούν πολλά εμπόδια. Ο
εμβολιασμός προκαλεί την τοπική παραγωγή IgA αντισωμάτων στον κατώτερο γεννητικό
σωλήνα, ώστε να προληφθεί η μόλυνση από τον HPV. Η χρήση εμβολίου έχει αποδειχθεί
αποτελεσματική έναντι της φυσικής μετάδοσης του ιού των θηλωμάτων του στόματος
σε κυνηγετικά σκυλιά.(62) Άλλες μελέτες έχουν δείξει ότι οι στοματικοί, οι ενδορρινικοί
και οι ενδοκολπικοί εμβολιασμοί ήταν πολύ πιο αποτελεσματικοί στην πρόκληση
τοπικής ανοσίας, καθώς και στην παραγωγή IgG αντισωμάτων μεγαλύτερης χημικής
συγγένειας, σε σχέση με τους παρεντερικούς εμβολιασμούς.(63-65)
Ένας δεύτερος προβληματισμός σχετικά με τη δημιουργία εμβολίου αφορά τους τύπους
του ιού που θα πρέπει να συμπεριληφθούν στη δομή του. Η απουσία διασταυρούμενης
αντίδρασης μεταξύ των IgG αντισωμάτων και των διαφόρων τύπων VLP πιθανόν να
καθιστά απαραίτητη τη δημιουργία ενός πολυδύναμου εμβολίου με διάφορους τύπους
VLP. Παρά το γεγονός ότι οι τύποι 16,18, 31 και 35 του HPV εντοπίζονται στο
80% των περιπτώσεων καρκίνου του τραχήλου της μήτρας, η ανοσοποίηση κατά των
ογκογόνων αυτών τύπων του ιού δεν παρέχει πλήρη προστασία από τον συγκεκριμένο
καρκίνο.(66) Επιπρόσθετα, οι τύποι του HPV που εντοπίζονται σε καρκινικές βλάβες
ποικίλουν από χώρα σε χώρα, και έτσι ένα εμβόλιο που έχει ως στόχο την πρόληψη
από τη νόσο σε ποσοστό 80%, πιθανόν να είναι αναποτελεσματικό σε μια συγκεκριμένη
περιοχή.(67)
Ένα άλλο ερώτημα που ανακύπτει είναι ποιες γυναίκες θα πρέπει να εμβολιαστούν.
Το οικονομικό κόστος για μαζικό εμβολιασμό υπολογίζεται πως θα είναι τεράστιο.
Πιστεύεται ότι ο εμβολιασμός των γυναικών υψηλού κινδύνου θα μείωνε σημαντικά
την εξάπλωση της νόσου, αλλά είναι αμφίβολο κατά πόσο θα μπορούσε να την εξαλείψει.
Μια εναλλακτική λύση είναι ο εμβολιασμός των κοριτσιών σχολικής ηλικίας πριν
την έναρξη της σεξουαλικής δραστηριότητάς τους. Σε αυτή την περίπτωση είναι
απαραίτητη η κατάλληλη στρατηγική ενθάρρυνσης των γονέων να εμβολιάσουν τις
έφηβες για την προστασία τους από ένα σεξουαλικώς μεταδιδόμενο νόσημα. Η ανάγκη
εμβολίου κατά του ιού των θηλωμάτων είναι ακόμη μεγαλύτερη στις αναπτυσσόμενες
χώρες, στις οποίες η συχνότητα του καρκίνου του τραχήλου είναι υψηλή και τα
διαγνωστικά και θεραπευτικά μέσα περιορισμένα.(68) Οι οικονομικές συνέπειες
του εμβολιασμού μεγάλου μέρους του πληθυσμού δεν θα πρέπει να υποτιμηθούν, καθώς
είναι ακόμη ασαφές το αν και πότε θα είναι δυνατό να αντικαταστήσει τα προγράμματα
screening του τραχήλου της μήτρας, ώστε να μειωθεί το κόστος.
Παράλληλα δεν είναι επακριβώς γνωστή η διάρκεια της ανοσίας που προκαλεί το
εμβόλιο. Μπορεί να χρειαστούν δυναμικοί εμβολιασμοί ανά δεκαετία, ώστε να διατηρηθεί
υψηλός τίτλος αδρανοποιητικών αντισωμάτων. Επιπρόσθετα, τα αδρανοποιητικά αυτά
αντισώματα από μόνα τους ίσως δεν παρέχουν μακροχρόνια ανοσία εναντίον του HPV.
Η καλύτερη στρατηγική συμπεριλαμβάνει τη χρήση υβριδικών E7 και L1/L2 VLΡ, αποτελεσματικών
στην πρόκληση παραγωγής αντισωμάτων, Τ-βοηθητικών και Τ-κυτταροτοξικών λεμφοκυττάρων
(CLT), τόσο με προληπτικές όσο και με θεραπευτικές ιδιότητες.(69)
Το χρονικό διάστημα μεταξύ της έναρξης της σεξουαλικής δραστηριότητας της γυναίκας
και της ανάπτυξης του καρκίνου του τραχήλου είναι συνήθως 30 χρόνια. Επιπλέον,
ο καρκίνος του τραχήλου προσβάλλει ένα πολύ μικρό ποσοστό σεξουαλικά ενεργών
γυναικών. Συνεπώς, η αποτελεσματικότητα μιας μελέτης προϋποθέτει τη στρατολόγηση,
τον εμβολιασμό και τη μετέπειτα μακροχρόνια παρακολούθηση χιλιάδων γυναικών,
προκειμένου να αποδειχθεί ότι ο εμβολιασμός προστατεύει από τον καρκίνο. Αντίθετα
μια μελέτη, η οποία θα αποδείκνυε την πρόκληση ειδικού τύπου ανοσίας έναντι
ενός συγκεκριμένου τύπου HPV ή τη σημαντική μείωση των περιστατικών CIN, θα
απαιτούσε τον έλεγχο ενός πολύ μικρότερου αριθμού ατόμων και θα οδηγούσε σε
συμπεράσματα σε πολύ μικρότερο χρονικό διάστημα.(70,71)
ΘΕΡΑΠΕΥΤΙΚΑ
ΕΜΒΟΛΙΑ
Μελέτες σε ζώα έχουν οδηγήσει στο συμπέρασμα ότι τα θεραπευτικά εμβόλια κατά
του HPV μπορεί να είναι αποτελεσματικά στην υποχώρηση της νόσου.(72) Την παρούσα
χρονική περίοδο δοκιμάζονται εμβόλια για την ανοσοποιητική ικανότητα και την
κλινική αποτελεσματικότητά τους στη φάση I και II κλινικών μελετών. Επειδή ο
HPV δεν είναι λυτικός ιός, τα θεραπευτικά εμβόλια πρέπει να ενεργοποιούν ανοσολογικούς
μηχανισμούς ικανούς να αναγνωρίζουν και να καταστρέφουν τα κύτταρα που έχουν
προσβληθεί από τον HPV. Πολλές μελέτες έχουν επικεντρώσει το ενδιαφέρον τους
στην πρόκληση παραγωγής ειδικών κυτταροτοξικών Τ-λεμφοκυττάρων έναντι συγκεκριμένων
πρωτεϊνών του ιού (πίνακας 1), η επιλογή των οποίων εξαρτάται από το επίπεδο
έκφρασής τους στις διάφορες στιβάδες του επιθηλίου κατά την εξέλιξη της λοίμωξης.
Οι πρωτεΐνες Ε1 και Ε2 του HPV μεταφράζονται στα αρχικά στάδια της λοίμωξης
και θα μπορούσαν να είναι ανοσολογικοί στόχοι σε εμβόλια, με σκοπό τον περιορισμό
της νόσου σε αρχικό στάδιο.(73-76) Οι πρωτεΐνες Ε6 και Ε7 μεταφράζονται καθ'
όλη τη διάρκεια εξέλιξης της HPV λοίμωξης, ακόμη και στα μεταλλαγμένα κύτταρα,
όπου η συνεχής έκφρασή τους είναι απαραίτητη για τη διατήρηση του κακοήθους
φαινότυπου.(77-79) Συνεπώς, οι Ε6 και Ε7 αποτελούν ειδικά αντιγόνα του όγκου,
και είναι πιθανό να αποτελέσουν χρήσιμους ανοσολογικούς στόχους για θεραπευτικά
εμβόλια, τα οποία στοχεύουν στη θεραπεία βλαβών υψηλού βαθμού κακοήθειας και
διηθητικών καρκινωμάτων.
Ο σχεδιασμός θεραπευτικών εμβολίων για τις HPV λοιμώξεις αντιμετωπίζει αρκετά
εμπόδια, τα οποία πρέπει να υπερκεραστούν. Κατ' αρχήν θα πρέπει να καθοριστούν
τα πλέον κατάλληλα αντιγόνα - στόχοι του ιού (πίνακας 1), καθώς και ο τρόπος
λήψης αυτών. Οι περισσότερες προσεγγίσεις επί του θέματος στηρίζονται στη γενικευμένη
ανοσολογική απάντηση στα ογκογονίδια Ε6 και Ε7, παρά το ότι δεν έχει αποδειχθεί
ότι τα αντιγόνα αυτά είναι σημαντικά στον φυσικό έλεγχο της HPV λοίμωξης. Τα
θεραπευτικά εμβόλια που στοχεύουν τα ογκογονίδια Ε6 και Ε7 εμφανίζουν τις καλύτερες
προοπτικές για τον έλεγχο της κακοήθειας από τον HPV. Σήμερα δοκιμάζονται οι
ογκοπρωτεΐνες Ε6 και Ε7 σε vectors (πεπτίδια και πρωτεΐνες), σε νουκλεϊνικά
οξέα, ή σε κυτταροεξαρτώμενα εμβόλια.(61)
Πολλά από τα υποψήφια εμβόλια υφίστανται βελτιώσεις, παράλληλα με την πρόοδο
της έρευνας των μεθόδων λήψης των αντιγόνων. Έχουν χρησιμοποιηθεί εμβόλια με
πεπτίδια(80-82) και πρωτεΐνες(83) ή εμβόλια που βασίζονται σε ιϊκά πλασμίδια(84)
και ιϊκό DNA.(85) Η χρήση ενός εμβολίου μεμονωμένα πιθανόν να μην αρκεί για
την καταστροφή όλων των προσβεβλημένων από τον HPV κυττάρων και διερευνάται
η ιδέα χρησιμοποίησης δύο διαφορετικών εμβολίων με συνεργική δράση. Πρωτογενή
προγράμματα ανοσοποίησης, στα οποία η αρχική ανοσοποίηση με DNA εμβόλιο ακολουθείται
από μία ή περισσότερες ανοσοποιήσεις με ετερόλογο εμβόλιο, έχουν ενθαρρυντικά
αποτελέσματα και αναμένονται τα κλινικά αποτελέσματα.(86,87)
Προκειμένου να αποδειχθεί η κλινική αποτελεσματικότητα των θεραπευτικών εμβολίων,
απαιτείται κατάλληλη οργάνωση των κλινικών μελετών.(72) Επειδή δεν θα ήταν δεοντολογικά
σωστό να επιχειρηθεί η θεραπεία των τραχηλικών βλαβών υψηλού βαθμού κακοήθειας
με τη χρήση ενός εμβολίου με μη αποδεδειγμένη αποτελεσματικότητα, θα πρέπει
το εμβόλιο να δοκιμαστεί αρχικά ως επικουρικό μέσο θεραπείας, παρά ως εναλλακτική
θεραπευτική λύση. Σε ό,τι αφορά στη σοβαρή δυσπλασία CIN και τα καρκινώματα
του τραχήλου, η αποτελεσματικότητα του εμβολίου θα μπορούσε να αξιολογηθεί με
βάση την επανεμφάνιση της νόσου και την επιβίωση της ασθενούς, όμως η κλασική
θεραπεία θα παίξει τον κύριο ρόλο σε αυτά τα συμπεράσματα και πιθανόν να επικαλύψει
τη συνεισφορά του εμβολίου στον θεραπευτικό σχεδιασμό.
Η αιδοιϊκή ενδοεπιθηλιακή νεοπλασία (VIN) χαρακτηρίζεται από αλλοιώσεις που
έχουν σχέση με τον HPV και οι οποίες είναι εξαιρετικά ανθεκτικές στις συνήθεις
θεραπείες.(88) Η χειρουργική εξαίρεση ακρωτηριάζει τις γυναίκες και συχνά είναι
ανεπιτυχής. Αυτό έχει ως αποτέλεσμα οι γυναίκες να υποβάλλονται σε παρηγορητική
θεραπεία με συνεχείς βιοψίες και κλινικές εξετάσεις. Ο εμβολιασμός γυναικών
με υψηλού βαθμού VIN μπορεί να αποτελέσει αποδεικτικό στοιχείο της κλινικής
αποτελεσματικότητας της ανοσοποίησης, χωρίς την επιρροή επιπρόσθετης θεραπευτικής
παρέμβασης. Στο Μάντσεστερ της Μεγάλης Βρετανίας έχει αρχίσει η φάση II μιας
μελέτης, η οποία βασίζεται στη χορήγηση εμβολίου με ανασυνδυασμένο γενετικό
υλικό του ιού, το οποίο κωδικοποιεί τις τροποποιημένες πρωτεΐνες Ε6/Ε7 των τύπων
16/18 του HPV, με πρώιμα αισιόδοξα αποτελέσματα.
Η αποτελεσματική χρήση ενός εμβολίου για τη θεραπεία του διηθητικού καρκίνου
παρεμποδίζεται από την αυξανόμενη πιθανότητα ανοσοκαταστολής, συνεπεία της προϊούσας
πορείας της νόσου. Έχει αποδειχθεί ότι τα καρκινικά κύτταρα παράγουν αντιγόνα
HLA κλάσης Ι, με αποτέλεσμα την απώλεια της αντιγονοπαρουσίασης από το μείζον
σύμπλεγμα ιστοσυμβατότητας (MCH).(89) Αυτό σημαίνει πως κύτταρα με υψηλές συγκεντρώσεις
των πρωτεϊνών Ε6 και Ε7 του HPV πιθανώς να μην αναγνωρίζονται και να μην καταστρέφονται
από τα κυκλοφορούντα κυτταροτοξικά Τ-λεμφοκύτταρα. Συνεπώς, ένα θεραπευτικό
εμβόλιο μπορεί να είναι πιο αποτελεσματικό σε προκαρκινικές αλλοιώσεις παρά
στον διηθητικό καρκίνο του τραχήλου.
Ο εμβολιασμός γυναικών με χαμηλού βαθμού CIN αποτελεί επίσης πρόκληση στον σχεδιασμό
των κλινικών ερευνών. Περίπου το 80% των αλλοιώσεων της ήπιας τραχηλικής ενδοεπιθηλιακής
νεοπλασίας (CIN I) υποχωρεί αυτόματα(30) και συνεπώς για την απόδειξη της κλινικής
αποτελεσματικότητας του εμβολίου θα απαιτηθούν μελέτες μεγάλου αριθμού γυναικών
με μακροχρόνια παρακολούθηση. Το πλεονέκτημα αυτής της ομάδας ασθενών είναι
ότι μπορεί να χορηγηθεί μόνο το εμβόλιο και με προσεκτική παρακολούθηση να επιτευχθεί
η πρώιμη διάγνωση της νόσου, αποδεικνύοντας παράλληλα και την κλινική αποτελεσματικότητα
του εμβολίου χωρίς την επίδραση επιπρόσθετης θεραπείας.
Η μέτρηση της ειδικής κατά του HPV ανοσίας σε εμβολιασμένες ασθενείς δεν είναι
ακριβής.(90) Η κυτταρική ανοσία συνήθως υπολογίζεται με την απομόνωση, την κάθαρση
και την εξάπλωση των ειδικών κατά του HPV κυτταροτοξικών Τ-λεμφοκυττάρων in
vitro, πριν δοκιμαστεί η ικανότητά τους να καταστρέψουν τα προσβεβλημένα από
τον HPV κύτταρα. Οι αναλύσεις αυτές είναι απαιτητικές και χρονοβόρες και σταδιακά
αντικαθίστανται από σύγχρονες μεθόδους, οι οποίες προσδιορίζουν τον αριθμό των
ειδικών Τ-λεμφοκυττάρων, συμπεριλαμβανομένων και των μεθόδων προσδιορισμού της
γ-ιντερφερόνης (μέθοδος ELISPOT) και των τετραμερών HLA. Ωστόσο, δεν έχει αποσαφηνιστεί
ακόμη με ποιο μηχανισμό η μετρούμενη ανοσία έχει σχέση με αντιδράσεις σημαντικές
για τη δημιουργία κλινικών αποτελεσμάτων, αφού δεν υπάρχουν ανοσολογικά στοιχεία
σχετικά με τις λοιμώξεις που υποχωρούν φυσιολογικά. Επιπλέον, η μέτρηση της
ειδικής κατά του HPV ανοσίας με τη χρήση κυττάρων που απομονώνονται από τις
βλάβες πιθανόν να είναι πιο σωστή σε σχέση με τη χρήση κυττάρων που απομονώνονται
από το περιφερικό αίμα, αν και τέτοιου είδους πειράματα είναι δύσκολα.
Ο σχεδιασμός θεραπευτικών εμβολίων κατά των HPV λοιμώξεων έχει αποτελέσει αντικείμενο
εντατικών ερευνών εδώ και πολλά χρόνια. Ενώ τα πρώιμα αποτελέσματα των κλινικών
ερευνών είναι αισιόδοξα, η πρακτική εισαγωγή μίας ή περισσοτέρων μεθόδων ανοσοθεραπείας
στη ρουτίνα της κλινικής πράξης δεν έχει ακόμη πραγματοποιηθεί. Οι ιοί των θηλωμάτων
έχουν εξελιχθεί ταυτόχρονα με τα κύτταρα-ξενιστές τους εδώ και εκατομμύρια χρόνια,
και μέρος της αποτελεσματικότητάς τους είναι οι ειδικοί μηχανισμοί, οι οποίοι
τους καθιστούν ικανούς να "εξουδετερώνουν" τη φυσική ανοσία του ξενιστή.
Συνεπώς, προκειμένου η ανοσοθεραπεία να είναι επιτυχής, θα πρέπει να υπερκεραστούν
αυτοί οι μηχανισμοί δράσης των ιών. Η σχεδίαση θεραπευτικών εμβολίων απαιτεί
περαιτέρω μελέτες διερεύνησης τόσο των ιϊκών μηχανισμών αποφυγής του αμυντικού
συστήματος του ξενιστή, όσο και των ανοσολογικών παραγόντων που είναι σημαντικοί
για τον φυσικό έλεγχο των HPV λοιμώξεων.
Παρά το γεγονός ότι οι δυσχέρειες του σχεδιασμού ανοσοθεραπειών είναι πολλές,
υπάρχει αισιοδοξία και αναμένεται ότι στις επόμενες δεκαετίες θα σημειωθούν
σημαντικές αλλαγές στον τρόπο αντιμετώπισης του καρκίνου του τραχήλου και των
προκαρκινικών καταστάσεων. Ένα εμβόλιο κατά του ιού των θηλωμάτων, το οποίο
θα συμβάλλει τόσο στην πρόληψη της HPV λοίμωξης όσο και στην αντιμετώπιση της
ήδη εγκατεστημένης νόσου, θα επηρεάσει σημαντικά την καταπολέμηση του καρκίνου
του τραχήλου της μήτρας, που προσβάλλει εκατομμύρια γυναίκες σε όλο τον κόσμο.
Summary
Petropoulou VP, Petropoulos PV.
The use of vaccines in the prevention and treatment of cervical cancer.
Hellen Obstet Gynecol 17(1): 56-66, 2005
The strong association between high risk human papilloma virus (HPV) infection and cervical carcinoma has been established by the detection of HPV DNA in virtually all tumours. This association presents the exciting possibility that cervical cancer may be prevented or treated by vaccination. HPV L1 virus-like particles (VLPs) show great promise as prophylactic HPV vaccines in ongoing clinical trials, but L2-based preventative vaccines have yet to be tested in patients. Also other therapeutic vaccines targeting E6 and/or E7 may provide the best opportunity to control HPV associated malignancies. Various candidate therapeutic HPV vaccines are currently being tested, whereby E6 and/or E7 are administered in live vectors, as peptides or proteins, in nucleic acid form, as component of chimeric VLPs, or in cell-based vaccines. Αn effective prophylactic vaccine would obviate the need for population-based cervical screening programs, while therapeutic vaccination might provide an effective adjunct to or replacement for conventional treatment for benign and malignant cervical disease. While the challenges associated with the design and implementation of immunotherapies are numerous, optimism remains high and it is expected that the next few decades will witness a revolutionary change in the way we treat cervical cancer and its premalignant lesions. A papilloma virus vaccine that prevents HPV infection on the one hand and acts against established disease on the other hand, would have a profound impact on one of the major cancers affecting women globally.
Key words: HPV infection, cervical cancer, prophylactic vaccines, therapeutic vaccines.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Walboomers JM, Jacobs MV, Manos MM. Human papillomavirus is a necessary cause
of invasive cervical cancer worldwide. J Pathol 1999; 189:12-19.
2. Matthews RE. Third report of the International Committee on Taxonomy of Viruses.
Classification and nomenclature of viruses. Intervirology 1979; 12:129-296.
3. Pilotti S, Donghi R, Giarola M. Papillomavirus, p53 alteration and primary
carcinoma of the vulva. Eur J Cancer 1993; 29:924-925.
4. Arrand J. Molecular genetics of human papillomaviruses. In: PL Stern and
MA Stanley, Editors, Human Papillomaviruses and Cervical Cancer: Biology and
Immunology, Oxford University Press, Oxford 1994:28-40.
5. Pfister H, Fuchs PG. Papillomaviruses: particles, genome organization and
proteins. In: K Syrjanen, L Gissmann and LG Koss, Editors, Papillo-maviruses
and Human Disease, Springer-Verlag, Berlin 1987:1-18.
6. Stanley MA. Virus-keratinocyte interactions in the infectious cycle. In:
PL Stern and MA Stanley, Editors, Human Papillomaviruses and Cervical Cancer,
Oxford University Press, Oxford 1994:116-131.
7. Roden RB, Kirnbauer R, Jenson AB, Lowy DR, Schiller JT. Interaction of papillomaviruses
with the cell surface. J Virol 1994; 68:7260-7266.
8. Qi YM, Peng SW, Hengst K. Epithelial cells display separate receptors for
papillomavirus VLPs and for soluble L1 capsid protein. Virology 1996; 216:35-45.
9. Evander M, Frazer IH, Payne E, Qi YM, Hengst K, McMillan NAJ. Identification
of the alpha(6) integrin as a candidate receptor for papillo-maviruses. J Virol
1997; 71:2449-2456.
10. JS Liu, SR Kuo, TR Broker, LT Chow. The functions of human papillomavirus
type 11 E1, E2 and E2c proteins in cell-free DNA replication. J Biol Chem 1995;
270:27283-27291.
11. Sedman J, Stenlund A. Co-operative interaction between the initiator E1
and the transcriptional activator E2 is required for replicator specific DNA
replication of bovine papillomavirus in vivo and in vitro. EMBO J 1995; 14:6218-6228.
12. Sedman T, Sedman J, Stenlund A. Binding of the E1 and E2 proteins to the
origin of replication of bovine papillomavirus. J Virol 1997; 71:2887-2896.
13. McBride AA, Romanczuk H, Howley PM. The papillomavirus E2 regulatory proteins.
J Biol Chem 1991; 266:18411-18414.
14. Crook T, Vousden KH. HPV oncoprotein function. In: C Lacey, Editor, Papillomavrius
Reviews: Current Research on Papillomaviruses, Leeds University Press, Leeds
1996:55-60.
15. Stoler MH, Rhodes CR, Whitbeck A, Wolinsky SM, Chow LT, Broker TR. Human
papillomavirus type 16 and 18 gene expression in cervical neoplasias. Hum Pathol
1992; 23:117-128.
16. Durst M, Glitz D, Schneider A, zur Hausen H. Human papillomavirus type 16
(HPV 16) gene expression and DNA replication in cervical neoplasia: analysis
by in situ hybridization. Virology 1992; 189:132-140.
17. Doorbar J. The E4 proteins and their role in the viral life cycle. In: C
Lacey, Editor, Papillomavirus Reviews: Current Research on Papillomaviruses.
Leeds University Press, Leeds 1996:31-38.
18. Scheffner M, Werness BA, Huibregtse JM, Levine AJ, Howley PM. The E6 oncoprotein
encoded by human papillomavirus types 16 and 18 promotes the degradation of
p53. Cell 1990; 63:1129-1136.
19. Kessis TD, Slebos RJ, Nelson WG. Human papillomavirus 16 E6 expression disrupts
the p53-mediated cellular response to DNA damage. Proc Natl Acad Sci USA 1993;
90:3988-3992.
20. Chellappan S, Kraus VB, Kroger B. Adenovirus E1A, simian virus 40 tumor
antigen, and human papillomavirus E7 protein share the capacity to disrupt the
interaction between transcription factor E2F and the retinoblastoma gene product.
Proc Natl Acad Sci USA 1992; 89:4549-4553.
21. Schwarz E, Freese UK, Gissman L. Structure and transcription of HPV sequences
in cervical carcinoma cells. Nature 1985; 314:111-113.
22. el Awady MK, Kaplan JB, Ob SJ, Burk RD. Molecular analysis of integrated
human papillomavirus 16 sequences in the cervical cancer cell line SiHa. Virology
1987; 159:389-398.
23. Choo KB, Pan CC, Han SH. Integration of human papillomavirus type 16 into
cellular DNA of cervical carcinoma: preferential deletion of the E2 gene and
invariable retention of the long control region and the E6/E7 open reading frames.
Virology 1987; 161:259-261.
24. Romanczuk H, Howley PM. Disruption of either the E1 or the E2 regulatory
gene of human papillo-mavirus type 16 increases viral immortalization capacity.
Proc Natl Acad Sci USA 1992; 89:3159-3163.
25. McDougall JK. HPV immortalisation and trans-formation. In: C Lacey, Editor,
Papillomavirus Reviews: Current Research on Papillomaviruses. Leeds University
Press, Leeds 1996:47-53.
26. Watson M. HPV infection prophylactic vaccination and need for awareness.
Aventis Pasteur MSD Clinical Development Dept., Lyon, France, 2004.
27. Rozendaal L, Walboomers JMM, Van der Linden JC. High risk human papillomavirus
in cyto-morphological normal smears has a high predictive value for development
of severe dysplasia. Int J Cancer 1996; 68:766-769.
28. White AE, Livanos EM, Tlsty TD. Differential dis-ruption of genomic integrity
and cell cycle regulation in normal human fibroblasts by the HPV oncoproteins.
Genes Dev 1994; 8:666-677.
29. Schiffman MH. Epidemiology of cervical human papillomavirus infections.
In: H Zur Hausen, Editor, Human Pathogenic Papillomaviruses. Current Topics
in Microbiology and Immunology. Springer Verlag, Berlin 1994:55-81.
30. Syrjanen KJ. Natural history of genital human hapillomavirus infections.
In: C Lacey, Editor, Papillomavirus Reviews: Current Research on Papillomaviruses.
Leeds University Press, Leeds 1996:189-206.
31. Remmink AJ, Walboomers JMM, Helmerhorst TM. The presence of persistent high-risk
HPV genotypes in dysplastic cervical lesions is associated with progressive
disease: natural history up to 36 months. Int J Cancer 1995; 61:306-311.
32. Ho GY, Buck RD, Klein S. Persistent genital human papillomavirus infection
as a risk factor for persistent cervical dysplasia. J Nat Cancer Inst 1995;
87:1365-1371.
33. Mandic A, Vujkov T. Human papillomavirus vac-cine as a new way of preventing
cervical cancer: a dream or the future? Ann Oncol 2004; 15(2):197-200.
34. Lee AK, Eisinger M. Cell-mediated immunity (CMI) to human wart virus and
wart-associated tissue antigens. Clin Exp Immunol 1976; 26:419-424.
35. Chretien JH, Esswein JG, Garagusi VF. Decreased T cell levels in patients
with warts. Archs Dermatol 1978; 114:213-215.
36. Schneider V, Kay S, Lee HM. Immunosuppression as a high-risk factor in the
development of condy-loma accuminata and squamous neoplasia of the cervix. Acta
Cytol 1983; 27:220-224.
37. Halpert R, Fruchter RG, Seclus A, Butt K, Boyce JG, Sillman FH. HPV and
lower genital tract neoplasia in renal transplant patients. Obstet Gynecol 1985;
68:251-258.
38. Laga M, Icenogle JP, Marsella R. Genital papil-lomavirus infection and cervical
dysplasia-opportunistic complications of HIV infection. Int J Cancer 1992; 48:682-688.
39. Okabayashi M, Angell MG, Christensen ND, Kreider JW. Morphometric analysis
and identification of infiltrating leucocytes in regressing and progressing
Shope rabbit papillomas. Int J Cancer 1991; 49:919-923.
40. Coleman N, Birley HDL, Renton AM. Im-munological events in regressing genital
warts. Am J Clin Pathol 1994; 102:768-774.
41. Vardy DA, Baadsgaard O, Hansen ER, Lisby S, Vejlsgaard GL. The cellular
immune response to human papillomavirus infection. Int J Dermatol 1990; 29:603-610.
42. Kirnbauer R, Hubbert NL, Wheeler CM, Becker TM, Lowy DR, Schiller JT. A
virus-like particle enzyme-linked-immunosorbent -assay detects serum antibodies
in a majority of women infected with human papillomavirus type-16. J Nat Cancer
Inst 1994; 86:494-499.
43. Nonnenmacher B, Hubbert NL, Kirnbauer R. Serologic response to human papillomavirus
type 16 (HPV-16) virus-like particles in HPV-16 DNA-positive invasive cervical
cancer and cervical intraepithelial neoplasia grade III patients and controls
from Colombia and Spain. J Infect Dis 1995; 172:19-24.
44. Lutzner MA. Papillomavirus lesions in immu-nodepression and immuno- suppression.
Clin Dermatol 1985; 3:165-169.
45. Man S. Human cellular immune responses against human papillomaviruses in
cervical neoplasia. Expert Reviews in Molecular Medicine 1998:1462-3974.
46. Evans E-M, Man S, Evans AS, Borysiewicz LK. Infiltration of cervical cancer
tissue with human papillomavirus-specific cytotoxic T lymphocytes. Cancer Res
1997; 57:2943-2950.
47. Kadish AS, Ho GYF, Burk RD. Lymphopro-liferative responses to human papillomavirus
(HPV) type 16 proteins E6 and E7: outcome of HPV infection and associated neoplasia.
J Nat Cancer Inst 1997; 89:1285-1293.
48. Bontkes HJ, de Gruijl TD, Bijl A. Human papil-lomavirus type 16 E2-specific
T-helper lymphocyte responses in patients with cervical intraepithelial neoplasia.
J Gen Virol 1999; 80:2453-2459.
49. Man S, Fiander A. Immunology of human papil-lomavirus infection in lower
genital tract. Best Pract Res Clin Obstet Gynaecol 2001; 15:701.
50. Remoue F, Jacobs N, Miot V, Boniver J, Delvenne P. High intraepithelial
expression of estrogen and progesterone receptor in the transformation zone
of the uterine cervix. Am J Obstet Gynecol 2003; 189:6.
51. Oseu W, Peiler T, Ohlschlager P, et al. A DNA vaccine based on a shuffled
E7 oncogene of the human papilloma 16 (HPV16) induces E7-specific cytotoxic
T- cells but lacks transfer activity. Vaccine 2001; 19:4276.
52. Schiller JT, Lowy DR. Papillomavirus-like particles and HPV vaccine development.
Semin Cancer Biol 1996; 7:373-382.
53. Hines JF, Ghim SJ, Jenson AB. Prospects for human papillomavirus vaccine
development: emerging HPV vaccines. Curr Opin Obstet Gynecol 1998; 10:15-19.
54. Kirnbauer R, Booy F, Cheng N, Lowy DR, Schiller JT. Papillomavirus L1 major
capsid protein self-assembles into virus-like particles that are highly immunogenic.
Proc Nat Acad Sci USA 1992; 89:12180-12184.
55. Suzich JA, Ghim SJ, Palmer Hill FJ. Systemic immunization with papillomavirus
L1 protein completely prevents the development of viral mucosal papillomas.
Proc Natl Acad Sci USA 1995; 92:11553-11557.
56. Breitburd F, Kirnbauer R, Hubbert NL. Immu-nisation with virus-like particles
from cottontail rabbit papillomavirus (CRPV) can protect against experimental
CRPV infection. J Virol 1995; 69:3959-3963.
57. Kirnbauer R, Chandrachaud LM, O'Neill BW. Virus-like particles of bovine
papillomavirus type 4 in prophylactic and therapeutic immunisation. Virology
1996; 219:37-44.
58. Harro C, Pang Y, Roden R. Safety and immu-nogenicity trial in adult volunteers
of a human papillomavirus 16 L1 virus-like particle vaccine. J Nat Cancer Inst
2001; 93:284-292.
59. Garcia-Carranca A. Vaccines against human papil-lomavirus and perspectives
for the prevention and control of cervical cancer. Salud Publica Mex 2003; 45Suppl
3:S437-42.
60. Watson M. HPV infection prophylactic vaccination and need for awareness.
Aventis Pasteur MSD Clinical Development Dept., Lyon, France, 2004.
61. Roden R, Wu TC. Preventative and therapeutic vaccines for cervical cancer.
Expert Rev Vaccines 2003; 2(4):495-516.
62. Bell JA, Sundberg JP, Ghim SJ, Newson J, Jenson AB, Schlegel R. A formalin-inactivated
vaccine protects against mucosal papillomavirus infection: a canine model. Pathobiology
1994; 62:194-198.
63. Liu XS, Abdul Jabbar I, Qi YM, Frazer IH, Zhou J. Mucosal immunisation with
papillomavirus virus-like particles elicits systemic and mucosal immunity in
mice. Virology 1998; 252:39-45.
64. Balmelli C, Roden R, Potts A, Schiller J, De Grandi P, Nardelli Haefliger
D. Nasal immunization of mice with human papillomavirus type 16 virus-like particles
elicits neutralizing antibodies in mucosal secretions. J Virol 1998; 72:8220-8229.
65. Rose RC, Lane C, Wilson S, Suzich JA, Rybicki E, Williamson AL. Oral vaccination
of mice with human papillomavirus virus-like particles induces systemic virus-neutralizing
antibodies. Vaccine 1999; 17:2129-2135.
66. Bosch FX, Manos MM, Munoz N. Prevalence of human papillomavirus in cervical
cancer: a worldwide perspective. International biological study on cervical
cancer (IBSCC) Study Group. J Natl Cancer Inst 1995; 87:796-802.
67. Garnett G, Waddell H. Public Health Paradoxes and the epidemiological impact
of an HPV Vaccine. J Clin Virol 2000; 19:101-111.
68. Parkin DM, Pisani P, Ferlay J. Estimates of the worldwide incidence of 25
major cancers in 1990. Int J Cancer 1999; 80:827-841.
69. Greenstone HL, Nieland JD, deVisser KE. Chimeric papillomavirus virus-like
particles elicit anti-tumour immunity against the E7 oncoprotein in an HPV16
tumour model. Proc Nat Acad Sci USA 1998; 95:1800-1805.
70. Kibur M, af Geijerstamm V, Pukkala E. Attack rates of human papillomavirus
type 16 and cervical neoplasia in primiparous women and field trial designs
for HPV16 vaccination. Sex Transm Infect 2000; 76:13-17.
61. Ruffin MT, Ogaily MS, Johnston CM, Gregoire L, Lancaster WD, Brenner DE.
Surrogate endpoint biomarkers for cervical cancer chemopreventive trials. J
Cell Biochem Suppl 1995; 23:113-124.
72. Duggan-Keen M, Brown M, Stacey S, Stern P. Papillomavirus Vaccines. Front
Bioscience 1998; 3:1192-1208.
73. Frazer IH, Tindle RW. Cell mediated immunity to papillomaviruses. In: C
Lacey, Editor, Papillomavi-rus Reviews: Current Research on Papillomavi-ruses.
Leeds University Press, Leeds 1996:151-163.
74. Schwartz RH. Co stimulation of T lymphocytes: The role of CD28,CTLA-4, and
B7/BB1 in interleukin production and immunotherapy. Cell 1992; 71:1065-1068.
75. Boon T, Coulie PG, Van den Eynde B. Tumour antigens recognised by T cells.
Immunol Today 1997; 18:267-268.
76. Han R, Reed CA, Cladel NM, Christensen ND. Immunization of rabbits with
cottontail rabbit papillomavirus E1 and E2 genes: protective immunity induced
by gene gun-mediated intracutaneous delivery but not by intramuscular injection.
Vaccine 2000; 18:2937-2944.
77. Halbert CL, Demers GW, Galloway DA. The E7 gene of human papillomavirus
type 16 is sufficient for immortalization of human epithelial cells. J Virol
1991; 65:473-478.
78. Hudson JB, Bedell MA, McCance DJ, Laiminis LA. Immortalization and altered
differentiation of human keratinocytes in vitro by the E6 and E7 open reading
frames of human papillomavirus type 18. J Virol 1990; 64:519-526.
79. von Knebel Doeberitz M, Rittmuller C, zur Hausen H, Durst M. Inhibition
of tumorigenicity of cervical cancer cells in nude mice by HPV E6-E7 anti-sense
RNA. Int J Cancer 1992; 51:831-834.
80. Steller MA, Gurski KJ, Murakami M. Cell-mediated immunological responses
in cervical and vaginal cancer patients immunized with a lipidated epitope of
human papillomavirus type 16 E7. Clin Cancer Res 1998; 4:2103-2109.
81. Muderspach L, Wilczynski S, Roman L. A phase I trial of a human papillomavirus
(HPV) peptide vaccine for women with high-grade cervical and vulvar intraepithelial
neoplasia who are HPV 16 positive. Clin Cancer Res 2000; 6:3406-3416.
82. Thomson SA, Khanna R, Gardner J. Minimal epitopes expressed in a recombinant
polyepitope protein are processed and presented to CD8+ cytotoxic T cells: implications
for vaccine design. Proc Natl Acad Sci USA 1995; 92:5845-5849.
83. Frazer IH, Tindle RW, Fernando GJP. Safety and immunogenicity of HPV 16
E7/algammulin. In: RW Tindle, Editor, Vaccines for Human Papillomavirus Infection
and Anogenital Disease. R. G. Lands Company, Austin 1999:91-104.
84. Borysiewicz LK, Fiander A, Nimako M. A reco-mbinant vaccinia virus encoding
human papilloma-virus types 16 and 18, E6 and E7 proteins as immunotherapy for
cervical cancer. Lancet 1996; 347:1523-1527.
85. Donnelly JJ, Martinez D, Jansen KU, Ellis RW, Montgomery DL, Liu MA. Protection
against papil-lomavirus with a polynucleotide vaccine. J Infect Dis 1996; 173:314-320.
86. Hallez S, Detremmerie O, Giannouli C. Interleukin-12-secreting human papillomavirus
type 16-transformed cells provide a potent cancer vaccine that generates E7-directed
immunity. Int J Cancer 1999; 81:428-437.
87. Ramshaw IA, Ramsay AJ. The prime-boost strategy: exciting prospects for
improved vacci-nation. Immunol Today 2000; 21:163-165.
88. van Beurden M, ten Kate FJ, Smits HL. Multifocal vulvar intraepithelial
neoplasia grade III and multicentric lower genital tract neoplasia is asso-ciated
with transcriptionally active human papillo-mavirus. Cancer 1995; 75:2879-2884.
89. Keating PJ, Cromme FV, Duggan-Keen M. Frequency of down-regulation of individual
HLA-A and -B alleles in cervical carcinomas in relation to TAP-1 expression.
Br J Cancer 1995; 72:405-411.
90. Tindle RW. Human papillomavirus vaccines for cervical cancer. Curr Opin
Immunol 1996; 8:643-650.