ΕΝΔΙΑΦΕΡΟΥΣΑ ΠΕΡΙΠΤΩΣΗ
Ιδιοπαθής πνευμονική
υπέρταση:
Περιγραφή περίπτωσης
Ε. Ατσάλη[1]
Γ. Παπαδόπουλος[3]
Σ. Ράμμος[2]
Ε. Λαγκώνα[1]
Φ. Ψύχου[1]
[1]Α' Παιδιατρική
Κλινική Παν. Αθηνών Ν.Π. Αγία Σοφία
[2]Καρδιολογική Κλινική Ν.Π. Αγία Σοφία
[3]Παιδοκαρδιολογική Κλινική Ωνασείου
Καρδιολογικού κέντρου
Υποβλήθηκε: 10/10/2005
ΠΕΡΙΛΗΨΗ
Περιγράφεται κορίτσι ηλικίας 8,5 ετών, με βαριά ιδιοπαθή πνευμονική υπέρταση.
Η ασθενής προσήλθε με αίσθημα κόπωσης και συγκοπτικά επεισόδια. Η διάγνωση της
ιδιοπαθούς πνευμονικής υπέρτασης βασίστηκε στα ευρήματα του υπερηχοκαρδιογραφήματος
Doppler, τα οποία επιβεβαιώθηκαν με τον καρδιακό καθετηριασμό και τον αποκλεισμό
των αιτίων της δευτεροπαθούς πνευμονικής υπέρτασης. Η θεραπευτική προσπάθεια
με τη χορήγηση οξυγόνου, αντιπηκτικής αγωγής και αναστολέα των υποδοχέων της
ενδοθηλίνης (Bosentan) δεν απέδωσε. Στο θεραπευτικό σχήμα προστέθηκε sildenafil
με καλύτερα αποτελέσματα. Η ασθενής εντάχθηκε σε λίστα αναμονής για μεταμόσχευση
πνευμόνων. (Δελτ Α' Παιδ Κλιν Πανεπ Αθηνών 2005, 52(4):386-391)
Λέξεις ευρετηριασμού: ιδιοπαθής πνευμονική υπέρταση, bosentan, sildenafil.
ΕΙΣΑΓΩΓΗ
Η διάγνωση της πνευμονικής υπέρτασης τίθεται, όταν η μέση πίεση στην πνευμονική
αρτηρία είναι μεγαλύτερη των 25mmHg σε ηρεμία και των 30mmHg στην άσκηση.[1,4,9,11]
Η πίεση στην πνευμονική αρτηρία υπολογίζεται έμμεσα από την ταχύτητα ανάδρομης
ροής στην τριγλώχινα σε υπερηχοκαρδιογράφημα Doppler.[1,3,7]
Η πνευμονική υπέρταση διακρίνεται σε ιδιοπαθή και δευτεροπαθή. Η διάγνωση της
ιδιοπαθούς τίθεται εξ αποκλεισμού, όταν δεν ενοχοποιείται για την ανάπτυξή της
κάποιο νόσημα του πνευμονικού παρεγχύματος, του συνδετικού ιστού, της καρδιάς,
η χρόνια θρομβοεμβολική νόσος ή η λήψη φαρμάκων (κοκαΐνη, ανορεξιογόνα)[4,7,11]
(πίνακας 1).
Η ιδιοπαθής πνευμονική υπέρταση διακρίνεται σε οικογενή (6-10% των περιπτώσεων)
και σποραδική μορφή.[1,4] Η οικογενής μορφή μεταβιβάζεται με αυτόσωμο επικρατούντα
χαρακτήρα και ατελή διεισδυτικότητα.[1,4,7,9] Ένα από τα ενοχοποιούμενα γονίδια
εντοπίζεται στο χρωμόσωμα 2 (2q33) και προκαλεί ελαττωματική λειτουργία του
υποδοχέα BMPR2 (Bone Morphogenetic Protein Receptor type II).[5] Σημειώνεται
ότι η μετάλλαξη αυτή απαντάται στο 26% των σποραδικών περιπτώσεων σε ενηλίκους,[1,4,6,9]
γεγονός που αποδίδεται σε ατελή διεισδυτικότητα και νέες μεταλλάξεις. Άλλα δύο
γονίδια που σχετίζονται με τη νόσο έχουν εντοπισθεί στα χρωμοσώματα 2 (2q31)
και 12 (12q13).[9]
| ΠΙΝΑΚΑΣ 1. Ταξινόμηση πνευμονικής υπέρτασης (Παγκόσμια Οργάνωση Υγείας).[4] |
|
1η ομάδα: Πνευμονική
αρτηριακή υπέρταση |
| ΠΙΝΑΚΑΣ 2. Λειτουργικη ταξινομηση ασθενων με πνευμονικη υπερταση (New York Heart Association) | ||||
| Δραστηριότητα* Συμπτωματολογίαο |
Τάξη
Ι
|
Τάξη
ΙΙ
|
Τάξη
ΙΙΙ
|
Τάξη
ΙV
|
| * συνήθης (-) (+) * <συνήθη (+) * καμία (+) |
(-)
|
(+)
|
(+)
|
(+) |
| * κόπωση, δύσπνοια, αίσθημα παλμών, στηθάγχη | ||||
| ΠΙΝΑΚΑΣ 3. ελεγχος σε ασθενη με πνευμονικη υπερταση |
|
Βαλβιδοπάθεια - Ελλείμματα
κολποκοιλιακού διαφράγματος - Νόσημα αρ. καρδιακών κοιλοτήτων Νοσήματα αναπνευστικού
συστήματος υποξαιμία Πυλαιοπνευμονική υπέρταση
- Νοσήματα κολλαγόνου - ΑIDS - Xρόνια θρομβοεμβολική πνευμονική υπέρταση |
ΠΕΡΙΓΡΑΦΗ
ΠΕΡΙΠΤΩΣΗΣ
Κορίτσι, ηλικίας 8,5 ετών, εισήχθη στην κλινική μας λόγω αισθήματος κόπωσης
και επεισοδίων απώλειας συνείδησης. Επρόκειτο για το τρίτο παιδί φαινοτυπικά
υγιών γονέων με ελεύθερο κληρονομικό αναμνηστικό. Τα δύο αδέλφια της, ηλικίας
12 και 10 ετών, ήταν υγιή. Η ασθενής γεννήθηκε με βάρος 2900gr. Η περιγεννητική
περίοδος ήταν ελεύθερη. Τα προβλήματά της ξεκίνησαν πέντε μήνες πριν την εισαγωγή,
οπότε άρχισε να παραπονείται για έντονο αίσθημα κόπωσης και δύσπνοια, ιδιαίτερα
κατά την άσκηση. Δύο μήνες αργότερα παρουσίασε βήχα και κυάνωση των χειλέων
και στη συνέχεια τρία συγκοπτικά επεισόδια κατά τη διάρκεια άσκησης.
Κατά την εισαγωγή, στην αντικειμενική εξέταση διαπιστώθηκαν ακροκυάνωση, αρχόμενη
πληκτροδακτυλία, ιδιαίτερα αυξημένη ένταση του 2ου καρδιακού τόνου και συστολικό
φύσημα 3/6 ακουστό σε όλο το προκάρδιο, ιδιαίτερα στο αριστερό κάτω χείλος του
στέρνου. Από τον έλεγχο των υπόλοιπων συστημάτων δεν διαπιστώθηκε κάτι παθολογικό.
Το ιστορικό και τα ευρήματα της αντικειμενικής εξέτασης της ασθενούς κατηύθυναν
σε παθήσεις του αναπνευστικού ή του κυκλοφορικού συστήματος. Έγιναν, ως εκ τούτου,
ακτινογραφία θώρακα και καρδιολογική εκτίμηση (ΗΚΓφημα και υπερηχοκαρδιογράφημα
Doppler), τα οποία έθεσαν τη διάγνωση της πνευμονικής υπέρτασης.
Εργαστηριακός έλεγχος: Α/φία θώρακα: προβολή του κώνου της πνευμονικής αρτηρίας
και ελαττωμένη αιμάτωση στην περιφέρεια των πνευμόνων (εικόνα 1).
ΗΚΓφημα: εικόνα υπερτροφίας των δεξιών καρδιακών κοιλοτήτων (εκσεσημασμένη απόκλιση
του άξονα προς τα δεξιά, QRS +160ο, και strain δεξιάς κοιλίας).
Δυσδιάστατο Echo και Echo Doppler: χωρίς ανατομική καρδιακή ανωμαλία, ανάδρομη
ροή στην τριγλώχινα με ταχύτητα ροής 5m/sec, τιμή που αντιστοιχεί σε συστολική
πίεση στην πνευμονική αρτηρία 110mmHg (σοβαρού βαθμού πνευμονική υπέρταση).
Καθετηριασμός καρδιάς: πιέσεις στην πνευμονική κυκλοφορία σχεδόν ίσες με της
συστηματικής (96% της συστηματικής), μειωμένο SpO2 του αρτηριακού αίματος (93%)
χωρίς διαφυγή αίματος από την αριστερή στη δεξιά κοιλία, υπερτροφία της δεξιάς
κοιλίας και διάταση του στελέχους της πνευμονικής και των κλάδων της (εικόνα
2).
Διαχυτική ικανότητα CO: 65% της αναμενόμενης.
Ο έλεγχος θρομβοφιλίας ανέδειξε ομοζυγωτία για τη μετάλλαξη C T677 του ενζύμου
μεθυλενο-τετραϋδροφυλλική ρεδουκτάση.
Σπινθηρογράφημα αιμάτωσης πνευμόνων: μειωμένη διάχυση του ραδιοφαρμάκου στο
ανώτερο βρογχοπνευμονικό τμήμα του αριστερού πνεύμονα και ελαφρώς ανομοιογενής
διάχυση του ραδιοφαρμάκου στο δεξιό πνεύμονα.
Φυσιολογικά ήταν η μαγνητική αγγειογραφία του πνευμονικού αγγειακού δικτύου,
η αξονική τομογραφία του θώρακα υψηλής ευκρίνειας, η σπιρομέτρηση, ο υπόλοιπος
έλεγχος θρομβοφιλίας (FV Leiden, FII 20210Α, ATΙΙΙ, πρωτεΐνες C και S, Lpa,
επίπεδα ομοκυστεΐνης, d-dimers, lupus anticoagulant, αντισώματα καρδιολιπίνης,
β2GPI), η ηλεκτροφόρηση της αιμοσφαιρίνης, η θυρεοειδική λειτουργία, η μελέτη
ύπνου, ο έλεγχος με Doppler του σπληνοπυλαίου άξονα, και αρνητικά ο έλεγχος
αυτοαντισωμάτων (ΑΝΑ, αντι-DNA, SSA, SSB, Sm, URNP, SCL-70, αντικεντρομεριδιακά)
και τα αντισώματα έναντι HIV.
Με την ολοκλήρωση του ανωτέρω ελέγχου αποκλείστηκαν τα αίτια της δευτεροπαθούς
και τέθηκε η διάγνωση της ιδιοπαθούς πνευμονικής υπέρτασης. Έγινε σταδιοποίηση
της νόσου (Νew York Heart Association Functional Classification - πίνακας 2).
Η συμπτωματολογία του παιδιού εμφανιζόταν με δραστηριότητα μικρότερη από τη
συνηθισμένη και ταξινομήθηκε στην τάξη III. Ως μέτρο εκτίμησης της αποτελεσματικότητας
της χορηγούμενης αγωγής αποτέλεσε η δοκιμασία βάδισης 6 λεπτών. Στη δοκιμασία
αυτή το παιδί βάδισε 450m (με όριο φυσιολογικού τα 500m) εμφανίζοντας όμως έντονη
δύσπνοια.
Αμέσως μετά τη διάγνωση χορηγήθηκαν στην ασθενή αναστολέας των υποδοχέων ενδοθηλίνης
(Βosentan σε δόση 62,5mg/24ωρο για ένα μήνα και 62,5mgx2/24ωρο στη συνέχεια),
αντιπηκτική αγωγή και υποστηρικτικά οξυγόνο. Η τρίμηνη παρακολούθηση του παιδιού
έδειξε, όπως αποδείχτηκε με τη δοκιμασία βάδισης 6 λεπτών, φτωχή ανταπόκριση
στην αγωγή αυτή και αποφασίστηκαν συνδυασμένη χορήγηση αναστολέα των υποδοχέων
ενδοθηλίνης με sildenafil και ένταξη του παιδιού σε λίστα αναμονής για μεταμόσχευση
πνευμόνων.
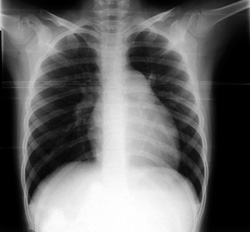
Eικόνα 1. Ακτινογραφία θώρακα της ασθενούς κατά την εισαγωγή.
Προβολή του κώνου της πνευμονικής αρτηρίας και ελαττωμένη αιμάτωση στην περιφέρεια
των πνευμόνων.
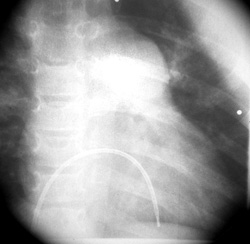
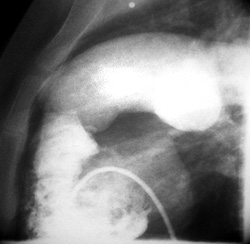
Εικόνα 2. Καθετηριασμός καρδιάς
της ασθενούς. Υπερτροφία δεξιάς κοιλίας και διάταση του στελέχους της πνευμονικής
αρτηρίας και των κλάδων της.
ΣΥΖΗΤΗΣΗ
Η ιδιοπαθής πνευμονική υπέρταση εμφανίζεται με συχνότητα 1-2/1.000.000,[1,9]
συχνότερα στις γυναίκες (Θ/Α 1,7).[3] Συνήθως εκδηλώνεται την 3η με 4η δεκαετία
της ζωής (μέση ηλικία 36,4 χρόνια), αναφέρεται όμως σπάνια ακόμη και σε παιδιά
βρεφικής ηλικίας.[7,9,11] Η ασθενής μας εμφάνισε τα πρώτα συμπτώματα της νόσου
στην ηλικία των 8 ετών και διαγνώσθηκε 5 μήνες από την έναρξη της συμπτωματολογίας.
Το αναφερόμενο μεσοδιάστημα στη βιβλιογραφία είναι περίπου δύο χρόνια.[13,14]
Η πνευμονική υπέρταση προβάλλει στους ενηλίκους συνήθως με δύσπνοια (60%).[1,3,4]
Τα συγκοπτικά επεισόδια τα οποία παρουσίασε η ασθενής μας, αμέσως μετά την έναρξη
της συμπτωματολογίας, είναι δείκτες της σοβαρής μείωσης του όγκου παλμού και
κακής πρόγνωσης.[3,11] Αποτελούν, σε αντίθεση με τους ενηλίκους, συχνό τρόπο
εμφάνισης της πνευμονικής υπέρτασης στα παιδιά, στα οποία αναφέρονται υψηλές
πιέσεις στην πνευμονική αρτηρία και κακή πρόγνωση.[1,3]
Ο εκτενής εργαστηριακός έλεγχος απέκλεισε στην ασθενή μας τις γνωστές αιτίες
πνευμονικής υπέρτασης, οδηγώντας στη διάγνωση της ιδιοπαθούς πνευμονικής υπέρτασης
(πίνακας 3). Συγκεκριμένα: 1. Με τον καθετηριασμό της καρδιάς αποκλείστηκαν
οι πρωτοπαθείς παθήσεις του κυκλοφορικού συστήματος.[4] 2. Με τη σπιρομέτρηση
και την αξονική θώρακος υψηλής ευκρίνειας αποκλείσθηκε η πιθανότητα πνευμονικού
νοσήματος.[7] 3. Η πυλαιοπνευμονική υπέρταση, το AIDS και η άπνοια κατά τον
ύπνο αποκλείστηκαν με τον ενδεδειγμένο εργαστηριακό έλεγχο.[7,11]
Η μειωμένη διαχυτική ικανότητα του CO με φυσιολογική σπιρομέτρηση, που παρατηρήθηκε
στην ασθενή μας, είναι εύρημα συμβατό με τη διαταραχή στο πνευμονικό αγγειακό
δίκτυο. Θα μπορούσε να αποδοθεί σε ιδιοπαθή πνευμονική υπέρταση,14 αλλά και
σε αυτοάνοσο νόσημα του συνδετικού ιστού[7] ή σε χρόνια θρομβοεμβολική νόσο.[16]
Η πιθανότητα αυτοάνοσου νοσήματος του συνδετικού ιστού αποκλείστηκε με βάση
το ιστορικό, την κλινική εικόνα της ασθενούς και την απουσία αυτοαντισωμάτων.[7]
Έτσι, η ιδιοπαθής πνευμονική υπέρταση και η χρόνια θρομβοεμβολική νόσος παρέμεναν
ως οι πιθανότερες αιτίες πνευμονικής υπέρτασης στην ασθενή μας.
Με τη διαπίστωση ότι το παιδί ήταν ομόζυγο για τη μετάλλαξη C T677 του ενζύμου
μεθυλενοτετραϋδροφυλλική ρεδουκτάση, μετάλλαξη η οποία συνδυάζεται συχνά με
αυξημένες τιμές ομοκυστεΐνης στο αίμα και αυξημένο ποσοστό θρομβώσεων στο αγγειακό
δίκτυο,15 έγινε προσδιορισμός της ομοκυστεΐνης στο αίμα της ασθενούς, που ήταν
φυσιολογικός. Το γεγονός αυτό απομάκρυνε τη διάγνωση της χρόνιας θρομβοεμβολικής
νόσου ως αιτίου της πνευμονικής υπέρτασης. Το γεγονός, όμως, ότι το σπινθηρογράφημα
αιμάτωσης δεν ήταν τυπικό ιδιοπαθούς πνευμονικής υπέρτασης, κατέστησε αναγκαία
την περαιτέρω διερεύνηση του πνευμονικού αγγειακού δικτύου με μαγνητική αγγειογραφία,
η οποία απέβη φυσιολογική, αποκλείοντας έτσι τη χρόνια θρομβοεμβολική νόσο.[7,11]
Η ασθενής μας δεν είχε επιβαρυμένο κληρονομικό αναμνηστικό και οι γονείς της
αρνήθηκαν να γίνει γενετικός ή άλλος έλεγχος της οικογένειας. Θα πρέπει πάντως
να σημειωθεί ότι σε πρόσφατη μελέτη κανένα από τα 13 παιδιά, ηλικίας 6 μηνών
- 13 ετών, με ιδιοπαθή πνευμονική υπέρταση δεν είχε μετάλλαξη σε κάποιο από
τα ενοχοποιούμενα γονίδια (2q33, 2q31, 12q13), καίτοι οι γονείς τους ή και άλλα
μέλη των οικογενειών τους παρουσίαζαν παθολογική αύξηση της πίεσης στην πνευμονική
αρτηρία κατά την άσκηση.[14]
Η χορήγηση αγγειοδιασταλτικών σε συνδυασμό με αντιπηκτική αγωγή (συνήθως βαρφαρίνη)
αποτελεί τη βασική γραμμή αντιμετώπισης της ιδιοπαθούς πνευμονικής υπέρτασης.[8]
Τα χορηγούμενα αγγειοδιασταλτικά περιλαμβάνουν: α) τους ανταγωνιστές ασβεστίου,
νιφεδιπίνη και διλτιαζέμη, στους οποίους, όμως, ανταποκρίνεται το 40% των ασθενών,[3]
β) την εποπροστενόλη και άλλα ανάλογα προστακυκλίνης,[8] τα οποία συνήθως χορηγούνται
με συνεχή iv έγχυση μέσω μόνιμα τοποθετημένου κεντρικού φλεβικού καθετήρα, και
τέλος γ) τους ανταγωνιστές των υποδοχέων ενδοθηλίνης όπως το bosentan - μη εκλεκτικός
ανταγωνιστής- και το υπό μελέτη ακόμη Sitaxsentan -εκλεκτικός ανταγωνιστής των
ΕΤΑ υποδοχέων ενδοθηλίνης.[8] Οι αναστολείς της φωσφοδιεστεράσης (Sildenafil
- Viagra) έχουν αρχίσει πρόσφατα να δοκιμάζονται στη θεραπεία της ιδιοπαθούς
πνευμονικής υπέρτασης με καλά αποτελέσματα.[10] Σε συνδυασμό με την ανωτέρω
αγωγή χορηγούνται υποστηρικτικά και κατά περίπτωση οξυγόνο, διουρητικά και καρδιοτόνωση.[1,13]
Η επιλογή έναρξης αγωγής στην ασθενή μας με ανταγωνιστές των υποδοχέων ενδοθηλίνης
οφειλόταν, σε μεγάλο βαθμό, στη δυσκολία χορήγησης εποπροστενόλης (συνεχής iv
χορήγηση σε ένα παιδί αυτής της ηλικίας και ανάγκη συχνής αναπροσαρμογής της
χορηγούμενης δόσης[1,13]). Η μη ανταπόκριση κατέστησε αναγκαία τη συγχορήγηση
Sildenafil, αλλά και την ένταξη του παιδιού σε λίστα μεταμόσχευσης πνευμόνων,
η οποία αποτελεί το έσχατο μέτρο αντιμετώπισης των ασθενών τάξης III ή IV (Νew
York Heart Association Functional Classification- πίνακας 2) που δεν ανταποκρίθηκαν
στη χορηγούμενη φαρμακευτική αγωγή μετά από 3-6 μήνες.[10]
Η πρόγνωση των ασθενών με ιδιοπαθή πνευμονική υπέρταση είναι ιδιαίτερα κακή.
Η μέση επιβίωση μετά τη διάγνωση είναι 3 περίπου χρόνια για τους ενηλίκους και
10 μήνες για τα παιδιά,8 με κύριο προγνωστικό παράγοντα τη λειτουργική τάξη
στην οποία ταξινομούνται. Η πιο συχνή αιτία θανάτου παραμένει η προοδευτική
εμφάνιση δεξιάς καρδιακής ανεπάρκειας, που ακολουθείται από αιφνίδιο θάνατο.[13]
Η ασθενής μας έχει, όπως συμπεραίνεται από τα ανωτέρω, βαριά ιδιοπαθή πνευμονική
υπέρταση και η πρόγνωσή της είναι κακή.
Idiopathic
pulmonary hypertension
E. Atsali, G. Papadopoulos, S. Rammos, E. Langona, F. Psychou
(Ann Clin Paediatr 2005; 52(4):386-391)
An 8,5 year old girl with severe primary pulmonary hypertension is described. Τhe patient presented with fatigue and repeated syncope. Pulmonary hypertension was detected by Doppler echocardiography and was confirmed by cardiac catheterization. Causes of secondary pulmonary hypertension were excluded by appropriate testing. Therapy with home oxygen, warfarin and endothelin-receptor antagonists (Bosentan) failed. Sildenafil was added to treatment with better results. The patient was listed for lung transplantation.
Key words: idiopathic pulmonary hypertension, bosentan, sildenafil.
ΒΙΒΛΙΟΓΡΑΦΙΑ
1. Haworth SG. Primary pulmonary hypertension in childhood. Arch Dis Child 1998;
79:452-5.
2. Bossone E, Rubenfire M, Bach DS, Ricciardi M, Armstrong WF. Range of tricuspid
regurgitation velocity at rest and during exercise in normal adult men: implications
for the diagnosis of pulmonary hypertension. J Am Coll Cardiol 1999; 33:1662-3.
3. Sandoval J, Bauerle O, Gomez A, Palomar A, Martinez, Guerra ML, et al. Primary
pulmonary hypertension in children: clinical characterization and survival.
J Am Coll Cardiol 1995; 25:466-74
4. Farber HW, Loscalzo J. Pulmonary arterial hypertension. N Engl J Med 2004;
351:1655-65.
5. Deng Z, Morse JH, Slager SL, Cuervo N, Moore KJ, Venetos G, et al. Familial
primary pulmonary hypertension (gene PPH1) is caused by mutations in the bone
morphogenetic protein receptor-II gene. Am J Hum Genet 2000; 67:737-44.
6. Thomson JR, Machado RD, Pauciulo MW, Morgan NV, Humbert M, Elliott GC, et
al. Sporadic primary pulmonary hypertension is associated with germline mutations
of the gene encoding BMPR-II, a receptor member of the TGF-beta family. J Med
Genet 2000; 37:741-5.
7. Μc Goon M, Gutterman D, Steen V, Barst R, McCrory DC, Fortin TA, et al. Screening,
early detection, and diagnosis of pulmonary arterial hypertension. ACCP evidence-based
clinical practice guidelines. Chest 2004; 126:14S-34S.
8. Badesch DB, Abman SH, Ahearn SH, Barst RJ, McCrory DC, Simonneau G, et al.
Medical therapy for pulmonary arterial hypertension. ACCP evidence-based clinical
practice guidelines. Chest 2004; 126:35S-62S.
9. Janssen B, Rindermann M, Barth U, Miltenberger-Miltenyi G, Mereles D, Abushi
A, et al. Linkage analysis in a large family with primary pulmonary hypertension:
genetic heterogeneity and a second PPH locus on 2q31-32. Chest 2002; 121:54S-56S.
10. Ηumbert M, Sitbon O, Simonneau G. Treatment of pulmonary arterial hypertension.
N Engl J Med 2004; 351:1425-36.
11. Gronig E, Koehler R, Miltenberger-Miltenyi G, Zimmermann R, Gorenflo M,
Mereles D, et al. Primary pulmonary hypertension in children may have a different
genetic background than in adults. Pediatric Res 2004; 56:571-578.
12. Karatza AA, Bush A, Magee AG. Safety and efficacy of Sildenafil therapy
in children with pulmonary hypertension. Int J Cardiol 2005; 20:267-73.
13. Rubin LJ. Primary Pulmonary Hypertension. N Eng J Med 1997; 336(2):111-7.
14. Runo JR, Loyd JE. Primary Pulmonary Hypertension. Lancet 2003; 361:1533-44.
15. Choi BO, et al. Homozygous C677T mutation in the MTHFR gene as an independent
risk factor for multiple small artery occlusions. Thrombosis Research 2003;
111:39-44.
16. Enright PL. Diffusing capacity for carbon monoxide. Available from: www.uptodate.com